
把2.1g的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加( )
|
| A. | 7.2g | B. | 3.6g | C. | 2.1g | D. | 无法确定 |
| 有关混合物反应的计算;钠的重要化合物. | |
| 分析: | CO在氧气中完全燃烧生成CO2,CO2和再与Na2O2反应,方程式为2CO+O2 H2在氧气中完全燃烧,生成H2O,H2O再与Na2O2反应,方程式为2H2+O2 |
| 解答: | 解:CO在氧气中完全燃烧生成CO2,CO2和再与Na2O2反应,方程式为2CO+O2 H2在氧气中完全燃烧,生成H2O,H2O再与Na2O2反应,方程式为2H2+O2 故由2.1gCO和H2组成的混合物在足量的O2中充分燃烧,立即通入足量的Na2O2固体,固体质量增加应为CO和H2的质量,即为2.1g, 故选C. |
| 点评: | 本题考查钠的重要化合物的性质、混合物计算等,侧重于学生的分析能力和计算能力的考查,注意总反应方程式的利用,也可以利用差量法进行判断,难度中等. |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
捕碳技术(主要指捕获CO2)在降低温 室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已被用作工业捕碳剂,其中一个可逆反应为(NH4)2
室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已被用作工业捕碳剂,其中一个可逆反应为(NH4)2 CO3(aq)+H2O(l)+CO2(g)
CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) ΔH3,为研究温度对(
2NH4HCO3(aq) ΔH3,为研究温度对( NH4)2CO3捕获CO2效率的影响,在某
NH4)2CO3捕获CO2效率的影响,在某 温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定
温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定 量的CO2气体(用氮气作为稀释剂),在t时
量的CO2气体(用氮气作为稀释剂),在t时 刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,得到趋势图(见图1)。则:
刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,得到趋势图(见图1)。则:
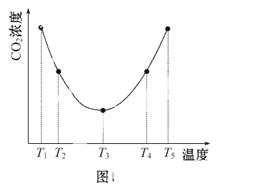
①ΔH3 0(填“>”“=”或“<”)。
②在T1~T2及T4~T5二个温度区间,容器内CO2气体浓度呈现如 图1所示的变化趋势,其原因是_______________________________________________________________________________。
图1所示的变化趋势,其原因是_______________________________________________________________________________。
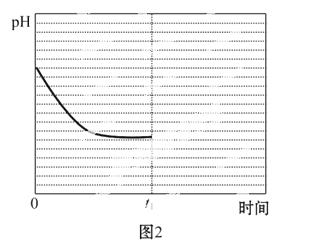
③此反应在温度为T1时,溶液pH随时间变化的趋势曲线如图2所示。当时间到达t1时,将该反应体系温度迅速上升到T2,并维持该温度。请在该图中画出t1时刻后溶液的pH变化总趋势曲线。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作的叙述不正确的是( )
|
| A. | 用干燥、洁净的玻璃棒醮取待测液滴在 pH试纸(置于表面皿内)上测溶液的pH |
|
| B. | 烧瓶、锥形瓶、烧杯加热时都要垫石棉网 |
|
| C. | 制备Fe(OH)3胶体时,应往沸水中加饱和FeC13溶液,并继续加热至溶液呈现红褐色为止 |
|
| D. | 已知I3﹣⇌I2+I﹣,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA
B. 标准状况下,14 g氮气含有的核外电子数为5NA
C. 标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
D. 标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关分散系的说法正确的是( )
|
| A. | 根据能否发生丁达尔效应将分散系分为浊液、溶液和胶体 |
|
| B. | 在Fe(OH)3胶体中加入过量盐酸不溶解 |
|
| C. | “血液透析”原理同溶液中固体颗粒的过滤原理相似 |
|
| D. | 除加入电解质可使胶体聚沉外,将两种带相反电荷胶粒的胶体混合也能发生聚沉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应的反应物和产物如下,如果该化学方程式中S和H2SO4的系数分别是5和1
(1)请配平下面的化学方程式:
CuS+ HNO3= Cu(NO3)2+ S+ H2SO4+ NO+ H2O
(2)该反应中,发生氧化反应的物质是 ,发生还原反应的物质是 .
(3)反应中,1mol 还原剂 (选填“得到”或“失去”) mol电子.
(4)如在标准状况下,反应产生336mL气体,则转移的电子数为 个.
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与科学、技术、社会、环境密切相关,下列有关说法不正确的是 ( )
A.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康有很大影响
B.福岛核电站泄漏的放射性物质131I和127I互为同位素,化学性质几乎相同
C.在黑夜中,我们能看到一束汽车的灯光,是因为我们生活中的大气是胶体体系
D.铝制品在空气中不易被腐蚀是因为铝的性质不活泼
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com