
【题目】乙烯是合成纤维、合成橡胶、合成塑料、合成乙醇的基本化工原料。回答下列问题:
(1)实验室快速制取少量乙烯可用乙烯利(![]() )与NaOH溶液反应制取。写出该反应的化学方程式为________(磷转化为磷酸正盐)。
)与NaOH溶液反应制取。写出该反应的化学方程式为________(磷转化为磷酸正盐)。
(2)乙烷裂解制备乙烯越来越受到石化企业的重视。已知部分热化学方程式如下:
Ⅰ.C2H6(g)=C2H4(g)+H2(g) △H1=+137kJ·mol-1
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+42kJ·mol-1
Ⅲ.C2H6(g)+CO2(g)=C2H4(g)+CO(g)+H2O(g) △H3
①反应Ⅲ的△H3=________kJ·mol-1。
②若在1273K时,100kPa下反应(Ⅰ)达到平衡时,混合气体中C2H4、C2H6、H2的物质的量分别为0.047、0.006、0.047,则乙烯的分压为p(C2H4)=________kPa;平衡常数Kp=________(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
③恒温恒容密闭容器中进行的反应(Ⅱ),能说明已达到平衡状态的是________(填字母)。
a.压强不再随时间变化 b.混合气体密度不再随时间变化
c.v(H2)正=v(CO)逆 d.单位时间内断裂C=O的数目与断裂H-O的相等
④乙烷直接裂解以及与CO2耦合裂解可能发生的反应及平衡转化率(α)与温度(T)的关系分别如下图所示,已知:a.C2H6=C2H4+H2;b.C2H6+CO2=C2H4+CO+H2O;c.C2H6+2CO2=4CO+H2;d.2C2H6+CO2=C2H4+2CO+2H2+CH4;e.16C2H6+9CO2=14C2H4+12CO+12H2+6H2O+CH4。

下列说法正确的是________(填字母)。
a.600℃以下,反应a的趋势最大
b.CO2和C2H6耦合裂解有利于提高乙烷的平衡转化率
c.过量CO2和C2H6耦合高温裂解,可较好防止催化剂表面结炭
d.用合适的催化剂催化CO2和C2H6耦合裂解,可提高反应平衡常数
(3)以太阳能电池为电源,利用电解法也可实现CO2制备乙烯,其装置如图所示。电极a为电源的________(填“正极”或“负极”),生成乙烯的电极反应式为________。

【答案】![]() +179 47 368.2 cd bc 负极 2CO2+12H++12e-=CH2=CH2+4H2O
+179 47 368.2 cd bc 负极 2CO2+12H++12e-=CH2=CH2+4H2O
【解析】
(2)①利用盖斯定律;
②分压=物质的量分数![]() 总压,代入平衡常数表达式可解;
总压,代入平衡常数表达式可解;
③紧扣“逆向相等,变量不变”判断平衡状态;
(3)与电源负极相连的是阴极,得到电子,发生还原反应。
(1)用![]() 与NaOH溶液反应制取少量乙烯,且磷转化为磷酸正盐即Na3PO4。综上该反应的化学方程式为:
与NaOH溶液反应制取少量乙烯,且磷转化为磷酸正盐即Na3PO4。综上该反应的化学方程式为:![]() ;
;
(2)①反应Ⅲ=反应Ⅰ+反应Ⅱ,则△H3=△H1+△H2=+179kJ·mol-1。
②在1273K时,100kPa下反应(Ⅰ)达到平衡时,混合气体中C2H4、C2H6、H2的物质的量分别为0.047、0.006、0.047,乙烯的分压为p(C2H4)=![]() =
=
47kPa;p(C2H6)=6 kPa,p(H2)=47kPa,平衡常数Kp=![]() =368.2 kPa;
=368.2 kPa;
③a.反应(Ⅱ)反应前后气体数目不变,压强一直恒定,故压强不再随时间变化不能说明已达到平衡状态,故a错误;
b.反应物和生成物全是气体,由质量守恒可知气体质量不变。且恒容密闭容器,由密度=气体质量![]() 容器体积,可知密度一直恒定,故混合气体密度不再随时间变化不能说明已达到平衡状态,故b错误;
容器体积,可知密度一直恒定,故混合气体密度不再随时间变化不能说明已达到平衡状态,故b错误;
c.v(H2)正=v(CO)逆,一正一逆反应速率,且符合方程式的化学计量数之比,能说明已达到平衡状态,故c正确;
d.单位时间内断裂C=O(正反应方向)的数目与断裂H-O(逆反应方向)的相等,且符合方程式的断键数目之比,能说明已达到平衡状态,故d正确;
答案选cd。
④a.600℃以下,反应e的α(C2H6)最大,故反应e的趋势最大,故a错误;
b.CO2和C2H6耦合裂解,可将C2H6转化为其他气体燃料,如CO和CH4,有利于提高乙烷的平衡转化率,故b正确;
c.过量CO2和C高温会反应为CO,可较好防止催化剂表面结炭,故c正确;
d.平衡常数仅受温度影响,催化剂不会改变平衡常数,故d错误;
答案选bc。
(3)与电极a相连的电极上CO2转化为乙烯,碳元素的化合价降低,得到电子,发生还原反应,作为阴极,故电极a为电源的负极,生成乙烯的电极反应式为2CO2+12H++12e-=CH2=CH2+4H2O。


科目:高中化学 来源: 题型:
【题目】锌空气燃料电池可用作电动车电源,电解质溶液为KOH溶液,正向放电,逆向充电,总反应为:Zn+O2+4OH-+2H2O ![]() 2Zn(OH)42-,下列说法正确的是
2Zn(OH)42-,下列说法正确的是
A. 充电时,电解质溶液中K+向阳极移动
B. 充电时,电解质溶液中c(OH-)逐渐减小
C. 放电时,负极反应为:Zn+4OH--2e-===Zn(OH) 42-
D. 可用盐酸代替KOH作电解液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 在外加电流的阴极保护法中,须将被保护的钢铁设备与直流电源的负极相连
B. 反应H2S(g)+ZnO(s)===H2O(g)+ZnS(s)在一定条件下可自发进行,且ΔS<0,则ΔH>0
C. 常温常压,氢氧燃料电池工作消耗2.24 L O2时,转移电子的数目为0.4×6.02×1023
D. 常温下,Ksp[Cu(OH)2]=2.6×10-19,pH=10的含Cu2+的溶液中,c(Cu2+)≥2.6×10-11mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g) ![]() 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A. 催化剂V2O5不改变该反应的逆反应速率
B. 保持容器体积不变,通入稀有气体增大反应体系的压强,反应速率一定增大
C. 该反应是放热反应,降低温度将缩短反应达到平衡的时间
D. 在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=(c2-c1)/(t2-t1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)在0.4 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

(1)该混合液中,NaCl的物质的量为______mol,含溶质MgCl2的质量为________g。
(2)该混合液中CaCl2的物质的量为________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为________mol·L1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水中过量的氨氮(NH3和NH4+)会导致水体富营养化。某科研小组用NaClO氧化法处理氨氮废水。已知:①HClO的氧化性比NaClO强;②NH3比NH4+更易被氧化;③国家标准要求经处理过的氨氮废水pH要控制在6~9。
(1)pH=1.25时,NaClO可与NH4+反应生成N2等无污染物质,该反应的离子方程式为_____。
(2)进水pH对氨氮去除率和出水pH的影响如下图所示

①进水pH为1.25~2.75范围内,氨氮去除率随pH升高迅速下降的原因是_____
②进水pH为2.75~6.00范围内,氨氮去除率随pH升高而上升的原因是_____
③进水pH应控制在_____左右为宜。
(3)为研究空气对NaClO氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是_____(填字母)。
a.O2的氧化性比NaClO弱 b.O2氧化氨氮速率比NaClO慢
c.O2在溶液中溶解度比较小 d.空气中的N2进入溶液中
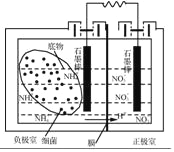
(4)利用微生物燃料电池可以对氨氮废水进行处理,其装置如图所示。闭合电路后,负极室与正极室均产生氮气,则负极室中NH4+发生反应的电极反应式为_____。该装置除了能对氨氮废水进行处理外,另一个突出的优点是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、铁及其化合物用途非常广泛。回答下列问题:
(1)基态S原子价电子排布式为________,基态Fe原子未成对电子数为________个。
(2)团簇 中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为________;与铁形成配位键的原子是________。
中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为________;与铁形成配位键的原子是________。
(3)工业上主要通过反应SO3+SCl2=SOCl2+SO2制备SOCl2(氯化亚砜),上述四种分子中,属于非极性分子的是________;SCl2分子空间构型为________形;SOCl2分子中心原子杂化方式是________。
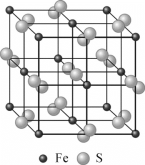
(4)黄铁矿的晶体结构如图所示,已知黄铁矿晶胞参数为a=0.5417nm,阿伏加德罗常数的值为NA。则黄铁矿的密度为________g·cm-3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法正确的是
A. 垃圾分类中可回收物标志:![]()
B. 农谚“雷雨肥庄稼”中固氮过程属于人工固氮
C. 绿色化学要求从源头上减少和消除工业生产对环境的污染
D. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒被誉为“合金的维生素”。从废钒(主要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如下图所示:

已知:
步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)![]() RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)
回答下列问题:
(1)步骤D酸浸过程中发生氧化还原反应的化学方程式为______________________。
(2)萃取时应加入适量碱的作用是___________________。
(3)步骤④中反应的离子方程式为___________________。
(4)步骤⑤加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<_____mol/L(按25℃计算,25℃时Ksp[Fe(OH)3]=2.6×10-39)。所得NH4VO3为离子化合物,NH4+的电子式为_______。
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为V0+,则V2O5与氢碘酸反应的离子方程式为_________________。
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=_______mol/L(萃取的量=![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com