
”¾ĢāÄæ”æĒė»Ų“šĻĀĮŠĪŹĢā:
(1)ĻÖÓŠÖŹĮæ±ČĪŖ11:14µÄCO2ŗĶCOµÄ»ģŗĻĘųĢ壬ŌņøĆ»ģŗĻĘųĢåÖŠµÄCO2ŗĶCOĪļÖŹµÄĮæÖ®±ČĪŖ_________£¬Ģ¼Ō×ÓŗĶŃõŌ×ÓµÄøöŹż±ČĪŖ________ £¬øĆ»ģŗĻĘųĢåµÄĦ¶ūÖŹĮæĪŖ__________ ”£
(2)12.4gŗ¬Na2XÖŠŗ¬Na+0.4mol£¬ŌņNa2XµÄĦ¶ūÖŹĮæŹĒ________ £¬XµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ____________”£
(3)ČĖŌģæÕĘų£ØŃõĘųŗĶŗ¤ĘųµÄ»ģŗĻĘų£©æÉÓĆÓŚ¼õĒįijŠ©¼²²”»ņ¹©ÉīĖ®Ē±Ė®Ō±Ź¹ÓĆ”£ŌŚ±ź×¼×“æöĻĀ£¬11.2LČĖŌģæÕĘųµÄÖŹĮæŹĒ4.8g£¬ĘäÖŠŃõĘųŗĶŗ¤ĘųµÄ·Ö×ÓŹżÖ®±ČŹĒ_____________,ŃõĘųµÄÖŹĮæŹĒ____________”£
”¾“š°ø”æ1£ŗ2 3£ŗ4 33.3g/mol 62g/mol 16 1£ŗ4 3.2g
”¾½āĪö”æ
£Ø1£©øł¾ŻĪļÖŹµÄĮ湫Ź½½ųŠŠ¼ĘĖć£»
£Ø2£©øł¾ŻÄ¦¶ūÖŹĮ湫Ź½½ųŠŠ¼ĘĖć£¬12.4gĪŖ0.2molNa2X£»
£Ø3£©ÉčĘųĢåĪļÖŹµÄĮæĪ“ÖŖŹż£¬ĮŠ·½³Ģ×é½ųŠŠ¼ĘĖć”£
(1)ĻÖÓŠÖŹĮæ±ČĪŖ11:14µÄCO2ŗĶCOµÄ»ģŗĻĘųĢ壬¶žŃõ»ÆĢ¼µÄĦ¶ūÖŹĮæĪŖ44g/mol£¬Ņ»Ńõ»ÆĢ¼µÄĦ¶ūÖŹĮæĪŖ28g/mol£¬ŌņøĆ»ģŗĻĘųĢåÖŠµÄCO2ŗĶCOĪļÖŹµÄĮæÖ®±ČĪŖ![]() =1£ŗ2£¬Ģ¼Ō×ÓŗĶŃõŌ×ÓµÄøöŹż±ČĪŖ£Ø1+2£©£ŗ£Ø2+2£©=3£ŗ4 £¬øĆ»ģŗĻĘųĢåµÄĦ¶ūÖŹĮæĪŖ
=1£ŗ2£¬Ģ¼Ō×ÓŗĶŃõŌ×ÓµÄøöŹż±ČĪŖ£Ø1+2£©£ŗ£Ø2+2£©=3£ŗ4 £¬øĆ»ģŗĻĘųĢåµÄĦ¶ūÖŹĮæĪŖ![]() ”£
ӣ
(2)12.4gŗ¬Na2XÖŠŗ¬Na+0.4mol£¬ĖµĆ÷Na2XµÄĪļÖŹµÄĮæĪŖ0.2mol£¬Ä¦¶ūÖŹĮæŹĒ![]() £¬XµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ62-2”Į23=16”£
£¬XµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ62-2”Į23=16”£
(3)ČĖŌģæÕĘų£ØŃõĘųŗĶŗ¤ĘųµÄ»ģŗĻĘų£©æÉÓĆÓŚ¼õĒįijŠ©¼²²”»ņ¹©ÉīĖ®Ē±Ė®Ō±Ź¹ÓĆ”£ŌŚ±ź×¼×“æöĻĀ£¬11.2LČĖŌģæÕĘųµÄĪļÖŹµÄĮæĪŖ0.5mol£¬ÖŹĮæŹĒ4.8g£¬ÉčŃõĘųĪļÖŹµÄĮæĪŖxmol£¬ŗ¤ĘųĪļÖŹµÄĮæĪŖymol£¬Ōņx+y=0.5£¬32x+4y=4.8£¬¼“x=0.1£¬y=0.4£¬ĘäÖŠŃõĘųŗĶŗ¤ĘųµÄ·Ö×ÓŹżÖ®±ČŹĒ1£ŗ4£¬ŃõĘųµÄÖŹĮæŹĒ0.1mol”Į32g/mol=3.2g”£


 Õć½ĆūŠ£ĆūŹ¦½š¾ķĻµĮŠ“š°ø
Õć½ĆūŠ£ĆūŹ¦½š¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒĪŅŠ£ŹµŃéŹŅ»ÆѧŹŌ¼ĮÅØĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ”£

ĻÖÓĆøĆÅØĮņĖįÅäÖĘ480mL1molL1µÄĻ”ĮņĖį”£æɹ©Ń”ÓƵÄŅĒĘ÷ÓŠ£ŗ¢Ł½ŗĶ·µĪ¹Ü£»¢Ś²£Į§°ō£»¢ŪÉÕ±£»¢ÜĮæĶ²”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ÅäÖĘĻ”ĮņĖįŹ±£¬»¹Č±ÉŁµÄŅĒĘ÷ÓŠ______(Š“ŅĒĘ÷Ćū³Ę)”£
(2)¾¼ĘĖć£¬ĖłŠčÅØĮņĖįµÄĢå»żŌ¼ĪŖ______mL£»Čō½«øĆĮņĖįÓėµČĢå»żµÄĖ®»ģŗĻ£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż______49%(Ģī”°>”±”¢”°<”±»ņ”°=”±)”£
(3)¶ŌĖłÅäÖʵÄĻ”ĮņĖį½ųŠŠ²ā¶Ø£¬·¢ĻÖĘäÅØ¶Č“óÓŚ1molL1£¬ÅäÖĘ¹ż³ĢÖŠĻĀĮŠø÷Ļī²Ł×÷æÉÄÜŅżĘšøĆĪó²īµÄŌŅņ______”£
¢ŁÓĆĮæĶ²ĮæČ”ÅØĮņĖįŹ±£¬ŃöŹÓæĢ¶ČĻß
¢ŚČŻĮæĘæÓĆÕōĮóĖ®Ļ“µÓŗóĪ“¾øÉŌļ
¢Ū½«Ļ”ŹĶŗóµÄĻ”ĮņĖįĮ¢¼“×ŖČėČŻĮæĘæŗó£¬Į¢¼“½ųŠŠŗóĆęµÄŹµŃé²Ł×÷
¢Ü×ŖŅĘČÜŅŗŹ±£¬²»É÷ÓŠÉŁĮæČÜŅŗČ÷³ö
¢Ż¶ØČŻŹ±£¬ø©ŹÓČŻĮæĘææĢ¶ČĻß
¢Ž¶ØČŻŗ󣬰ŃČŻĮæĘæµ¹ÖĆŅ”ŌČ£¬Õż·Åŗó·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ÓÖ²¹³ä¼øµĪĖ®ÖĮæĢ¶Č“¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠMgCl2ŗĶAl2(SO4)3µÄ»ģŗĻČÜŅŗ£¬ĻņĘäÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ£¬µĆµ½³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėNaOHµÄĪļÖŹµÄĮæ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņŌČÜŅŗÖŠCl£ ÓėSO42£µÄĪļÖŹµÄĮæÖ®±ČĪŖ
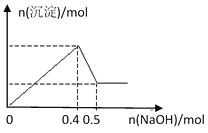
A. 1£ŗ3B. 1£ŗ6
C. 2£ŗ3D. 3£ŗ2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĢõ¼žĻĀ£¬½«4molNH3ŗĶ4molO2»ģŗĻÓŚ¹Ģ¶ØČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ4NH3(g)+5O2(g)=4X(g)+6H2O(g)”£2minŗóøĆ·“Ó¦“ļµ½Ę½ŗā£¬Éś³É3molH2O”£Ōņ£ŗ
(1)XµÄ»ÆѧŹ½ĪŖ___”£
(2)O2µÄ×Ŗ»ÆĀŹĪŖ___(O2×Ŗ»ÆĀŹ=ŅŃ·“Ó¦µÄO2µÄĮæ/O2µÄ×ÜĮæ”Į100%)”£
(3)0~2minÄŚ£¬v(NH3)=___mol”¤L-1”¤min-1”£
(4)Č¼ĮĻµē³ŲŹĒŅ»ÖÖøߊ§”¢»·¾³ÓŃŗĆŠĶ·¢µē×°ÖĆ”£Ņ»ÖÖČ¼ĮĻµē³ŲµÄµē½āÖŹČÜŅŗĪŖNaOHČÜŅŗ£¬øŗ¼«ĶØČėNH3£¬Õż¼«ĶØČėæÕĘų£¬²śĪļ¶Ō»·¾³ĪŽĪŪČ¾£¬Ōņøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ___£¬µēĀ·ÖŠĆæĶعż1molµē×Ó£¬Ļūŗıź×¼×“æöĻĀµÄæÕĘų___(¼ŁÉčæÕĘųÖŠO2µÄŗ¬ĮæĪŖ20%)L”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń£®ŹŅĪĀĻĀ£¬½«Ņ»ŌŖĖįHAµÄČÜŅŗŗĶKOHČÜŅŗµČĢå»ż»ģŗĻ£ØŗöĀŌ»ģŗĻŗóČÜŅŗµÄĢå»ż±ä»Æ£©£¬ŹµŃ鏿¾ŻČēĻĀ±ķ£ŗ
ŹµŃéŠņŗÅ | ĘšŹ¼ÅØ¶Č£Æ£Ømol”¤L£1£© | ·“Ó¦ŗóČÜŅŗµÄpH | |
c£ØHA£© | c£ØKOH£© | ||
¢Ł | 0£®1 | 0£®1 | 9 |
¢Ś | x | 0£®2 | 7 |
Ēė»Ų“š£ŗ
£Ø1£©HAČÜŅŗŗĶKOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____”£
£Ø2£©ĻĀĮŠ¹ŲÓŚ·“Ó¦ŗóµÄČÜŅŗĖµ·Ø²»ÕżČ·µÄŹĒ____£ØĢī×ÖÄø£©”£
a£®ŹµŃé¢Ś·“Ó¦ŗóČÜŅŗÖŠÖ»“ęŌŚ×ÅĮ½øöĘ½ŗā
b£®ŹµŃé¢Ś·“Ó¦ŗóČÜŅŗÖŠ£ŗc£ØA££©£«c£ØHA£©£¾0.1mol”¤L£1
c£®ŹµŃé¢Ś·“Ó¦ŗóČÜŅŗÖŠ£ŗc£ØK£«£©£½c£ØA££©£¾c£ØOH££©£½c£ØH£«£©
d£® ŹµŃé¢Ł·“Ó¦ŗóµÄČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØOH££©£½10-9mol”¤L£1£»x>0.2mol”¤L£1
¢ņ£®ŅŃÖŖ2H2£Øg£©£«O2£Øg£©£½2H2O£Ø1£© ¦¤H£½£572kJ”¤mol£1”£Ä³ĒāŃõČ¼ĮĻµē³ŲŅŌŹčĖɶąæ׏ÆÄ«°ōĪŖµē¼«£¬KOHČÜŅŗĪŖµē½āÖŹČÜŅŗ”£
£Ø3£©Š“³öøƵē³Ų¹¤×÷Ź±øŗ¼«µÄµē¼«·“Ó¦Ź½____”£
£Ø4£©ČōøĆĒāŃõČ¼ĮĻµē³ŲĆæŹĶ·Å228£®8kJµēÄÜŹ±£¬»įÉś³É1molŅŗĢ¬Ė®£¬ŌņøƵē³ŲµÄÄÜĮæ×Ŗ»ÆĀŹĪŖ____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĀÆĮ¶ĢśÖŠ·¢ÉśµÄ»ł±¾·“Ó¦Ö®Ņ»ČēĻĀ£ŗFeO(s)+CO(g) ”śFe(s)+CO2(g)-Q£¬ŅŃÖŖ1100”ꏱ£¬K=0.263
£Ø1£©Š“³öøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½____”£ĪĀ¶ČÉżøߣ¬»ÆŃ§Ę½ŗāŅʶÆŗó“ļµ½ŠĀµÄĘ½ŗā£¬øßĀÆÖŠCO2ŗĶCOµÄĢå»ż±ČÖµ___£¬Ę½ŗā³£ŹżKÖµ___£ØŅŌÉĻŃ”Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø2£©1100”ꏱ²āµĆøßĀÆÖŠc(CO2)=0025mol/L”¢c(CO)=0.1mol/L£¬ŌŚÕāÖÖĒéæöĻĀ£¬øĆ·“Ó¦ŹĒ·ń“¦ÓŚ»ÆŃ§Ę½ŗāדĢ¬___£ØŃ”Ģī”°ŹĒ”±»ņ”°·ń”±£©£¬“ĖŹ±£¬»Æѧ·“Ó¦ĖŁĀŹŹĒvÕż___vÄę£ØŃ”Ģī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©£¬ĘäŌŅņŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠŅ»»ģŗĻĪļµÄĖ®ČÜŅŗ£¬Ö»æÉÄÜŗ¬ÓŠŅŌĻĀĄė×ÓÖŠµÄČōøÉÖÖ£ŗK+”¢![]() ”¢Cl-”¢Mg2+”¢Ba2+”¢
ӢCl-ӢMg2+ӢBa2+Ӣ![]() Ӣ
”¢![]() £¬ĻÖȔȿ·Ż100mLČÜŅŗ½ųŠŠČēĻĀŹµŃé£ŗ
£¬ĻÖȔȿ·Ż100mLČÜŅŗ½ųŠŠČēĻĀŹµŃé£ŗ
(1)µŚŅ»·Ż¼ÓČėAgNO3ČÜŅŗÓŠ³Įµķ²śÉś£»
(2)µŚ¶ž·Ż¼Ó×ćĮæNaOHČÜŅŗ¼ÓČČŗó£¬ŹÕ¼Æµ½ĘųĢå0.04mol£»
(3)µŚČż·Ż¼Ó×ćĮæBaCl2ČÜŅŗŗ󣬵ĆøÉŌļ³Įµķ6.27g£¬¾×ćĮæŃĪĖįĻ“µÓ”¢øÉŌļŗ󣬳ĮµķÖŹĮæĪŖ2.33g”£øł¾ŻÉĻŹöŹµŃ飬ŅŌĻĀĶĘ²ā²»ÕżČ·µÄŹĒ
A.K+²»Ņ»¶Ø“ęŌŚB.100mLČÜŅŗÖŠŗ¬0.02mol![]()
C.Cl-²»Ņ»¶Ø“ęŌŚD.Ba2+”¢Mg2+²»“ęŌŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĻĀĮŠ·“Ó¦ÖŠ£¬Ė®¼Č²»ŹĒŃõ»Æ¼ĮÓÖ²»ŹĒ»¹Ō¼ĮµÄŹĒ( )
A.C+H2OØTCO+H2
B.2Na2O2+2H2OØT2NaOH+O2”ü
C.2Na+2H2OØT2NaOH+H2”ü
D.2F2+2H2OØT4HF+O2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøõŌŖĖŲ¼°Ęä»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠ¾ßÓŠ¹ć·ŗµÄÓĆĶ¾”£ŅŌijøõæóŹÆ(Ö÷ŅŖ³É·ÖŹĒCr2O3£¬ŗ¬Fe2O3”¢SiO2µČŌÓÖŹ)ĪŖŌĮĻÉś²śCr2O3µÄĮ÷³ĢČēĻĀ£ŗ
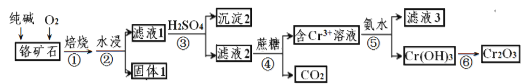
(1)Cr2O3ŌŚ±ŗÉÕŹ±Éś³ÉNa2CrO4£¬Š“³öµŚ¢Ł²½·¢ÉśµÄĖłÓŠ·½³ĢŹ½_________”£
(2)³Įµķ2µÄ»ÆѧŹ½ĪŖ_______”£
(3)²½Öč¢ŪÖŠCrO42-×Ŗ»Æ³ÉCr2O72- £¬Š“³öĘäĄė×Ó·½³ĢŹ½_______£¬ĮņĖįÄÜ·ń»»³ÉŃĪĖį²¢ĖµĆ÷ĘäĄķÓÉ______”£
(4)ĀĖŅŗ3ÖŠÖ÷ŅŖČÜÖŹµÄ»ÆѧŹ½ĪŖ____________”£
(5)CrO3µÄČČĪČ¶ØŠŌ½Ļ²ī£¬¼ÓČČŹ±Öš²½·Ö½ā£¬Ęä¹ĢĢ岊ĮōĀŹĖęĪĀ¶ČµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾£¬ŌņBµćŹ±øõµÄŃõ»ÆĪļ»ÆѧŹ½ĪŖ_______”£
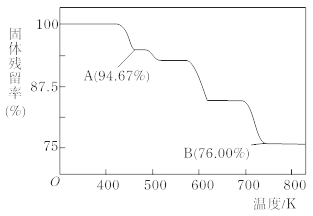
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com