
| A. | ①③④ | B. | ②⑤ | C. | ②③⑤ | D. | ②④ |
分析 用已知浓度的酸滴定未知浓度的碱时,c(碱)=$\frac{c(酸)•V(酸)}{V(碱)}$,若V(碱)偏大或V(酸)偏小,则导致待测碱液的浓度偏低,以此来解答.
解答 解:①酸式滴定管用蒸馏水洗后未用标准液润洗,标准液浓度偏小,造成V(酸)偏大,则浓度偏大,故错误;
②碱式滴定管用蒸馏水洗后,未用待测液润洗,则碱的浓度偏低,故正确;
③锥形瓶用蒸馏水洗后,用待测夜润洗,V(酸)偏大,则导致待测碱液的浓度偏高,故错误;
④滴定前酸式滴定管尖嘴部分有气泡,滴定过程中气泡消失,标准液体积读数增大,浓度偏高,故错误;
⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外,导致溶质损失,消耗的酸偏少,则浓度偏低,故正确.
故选B.
点评 本题考查酸碱中和滴定,为高频考点,把握酸碱的体积对浓度的影响为解答的关键,侧重分析与实验能力的考查,注意中和滴定原理,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.1mol•L-1•min-1 | B. | v(N2)=0.7 mol•L-1•min-1 | ||
| C. | v(NH3)=0.2mol•L-1•min-1 | D. | v(H2)=0.3mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
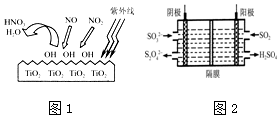
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2MnO2+2NH4++2e-═2MnO(OH)+2NH3 | B. | Zn-2e-═Zn2+ | ||
| C. | [Zn(NH3)2]2++2e-═Zn+2NH3 | D. | Mn4++e-═Mn3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两容器内压强一定相等 | B. | 两容器中A的浓度一定相等 | ||
| C. | 两容器吸收或放出的热量一定相等 | D. | 两容器中B的百分含量一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 70 mL | B. | 60mL | C. | 80 mL | D. | 128 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开始时观察到金属碎片表面有极少量气泡,可能原因为该金属片表面有氧化膜 | |
| B. | 过程中观察到金属碎片表面有大量气泡并在液面上“翻滚”,说明该合金碎片的密度小于该盐酸溶液的密度 | |
| C. | 该盐酸的物质的量浓度一定为4.0 mol•L-1 | |
| D. | 溶液X中Mg2+与Al3+的物质的量之比一定为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
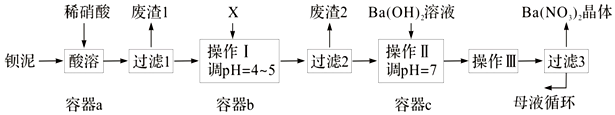
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有元素原子的最外层电子数都等于元素的最高化合价 | |
| B. | P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次减弱 | |
| C. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| D. | 熔融状态能导电的化合物一定含有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com