
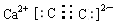 ,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2.
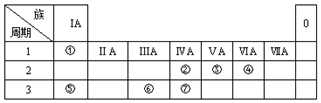
,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2.分析 由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大;非金属性越强,最高价含氧酸的酸性越强;
(2)由②、④、⑤三种元素组成的常见物质为Na2CO32-,CO32-水解溶液呈碱性;
(3)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,乙是一种常用的还原剂,则甲是C2 2-,乙是一氧化碳;
(4)⑦的气态氢化物为SiH4,燃烧发生反应:SiH4+2O2=SiO2+2H2O,转移1mol电子时,参加反应的SiH4为$\frac{1mol}{4-(-4)}$=0.125mol,计算1molSiH4燃烧放出的热量,注明物质的聚集状态与反应热书写热化学方程式;
(5)阳极上铝失电子生成铝离子,铝离子和碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体.
解答 解:由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,则原子半径:O<Al<Na;
非金属性Si<C<N,非金属性越强,最高价含氧酸的酸性越强,则酸性:H2SiO3<H2CO3<HNO3,
故答案为:O<Al<Na;H2SiO3<H2CO3<HNO3;
(2)由②、④、⑤三种元素组成的常见物质为Na2CO32-,CO32-水解溶液呈碱性,水解离子方程式为:CO32-+H2O?HCO3-+OH-,
故答案为:CO32-+H2O?HCO3-+OH-;
(3)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,乙是一种常用的还原剂,则甲是C2 2-,乙是一氧化碳,
碳化钙为离子化合物,其电子式为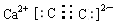 ;
;
高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳,反应的方程式为:3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2,
故答案为: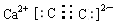 ; 3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2;
; 3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2;
(4)⑦的气态氢化物为SiH4,燃烧发生反应:SiH4+2O2=SiO2+2H2O,转移1mol电子时,参加反应的SiH4为$\frac{1mol}{4-(-4)}$=0.125mol,1molSiH4燃烧放出的热量为190.0kJ×$\frac{1mol}{0.125mol}$=1520.0 kJ,反应热化学方程式为:SiH4(g)+2O2(g)=SiO2(s)+2H2O(l)△H=-1520.0 kJ/mol,
故答案为:SiH4(g)+2O2(g)=SiO2(s)+2H2O(l)△H=-1520.0 kJ/mol;
(5)阳极上铝失电子生成铝离子,铝离子和碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,反应方程式为:Al-3e-=Al3+,Al3++3HCO3-═Al(OH)3↓+3CO2↑或Al-3e-+3HCO3-═Al(OH)3↓+3CO2↑,
故答案为:Al-3e-=Al3+,Al3++3HCO3-═Al(OH)3↓+3CO2↑或Al-3e-+3HCO3-═Al(OH)3↓+3CO2↑.
点评 本题考查位置、结构与性质关系的综合应用,题目难度中等,正确推断元素为解本题关键,注意结合物质的特殊性质来推断,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
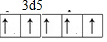 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学反应 | 平衡常数 | 温度(℃) | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O (g) | K3 | ||
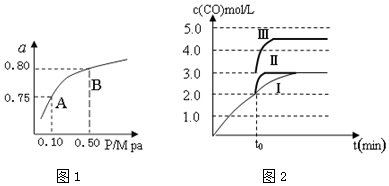
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测量中和热时不能用金属棒搅拌混合溶液 | |
| B. | 中和热不是一个定值,其大小由中和反应所消耗的酸和碱的多少决定 | |
| C. | 50mL0.5mol/LHCl和50mL0.55mol/LNaOH溶液反应测定中和热,计算式为△H=$\frac{4.18×100}{0.025}$×△tKJ/mol (注:△t-温度平均变化量) | |
| D. | 为了减少误差,量取稀NaOH溶液后,立即用同一个量筒量取稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
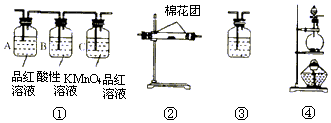 (1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式,并标出电子转移关系
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式,并标出电子转移关系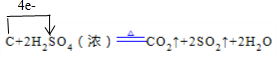 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氧化反应 | B. | 取代反应 | C. | 加成反应 | D. | 消去反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com