
| A. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为9NA | |
| B. | 标准状况下,2.24 L Cl2与氢氧化钠溶液完全反应转移电子数为0.1NA | |
| C. | 1 mol NaCl中含有6.02×1023个NaCl分子 | |
| D. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA |
分析 A、-OH不显电性;
B、求出氯气的物质的量,然后根据氯气和氢氧化钠溶液反应为歧化反应来分析;
C、氯化钠为离子晶体;
D、溶液体积不明确.
解答 解:A、-OH不显电性,故1mol-OH中含9NA个电子,而OH-中含10个电子,故1mol氢氧根中含10NA个电子,故A错误;
B、标况下2.24L氯气的物质的量为0.1mol,而氯气和氢氧化钠溶液反应为歧化反应,故0.1mol氯气反应转移0.1NA个电子,故B正确;
C、氯化钠为离子晶体,故氯化钠中无氯化钠分子,故C错误;
D、溶液体积不明确,故溶液中氢氧根的个数无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| X | SO2 | CO2 | CO2 | SO2 |
| Y | Cl2 | Cl2 | NH3 | H2S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
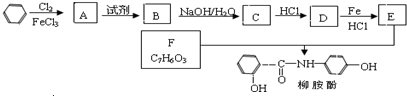

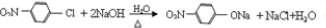 .
. .
.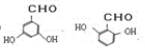 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2(SO4)3易溶于水,可用作净水剂 | |
| B. | Al2O3熔点高,可用作耐高温材料 | |
| C. | 铁比铜金属性强,可用FeCl3腐蚀Cu刻制印刷电路板 | |
| D. | NaHCO3溶于水呈碱性,可作抗酸药,服用时喝些醋能提高药效 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
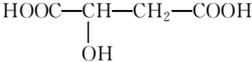
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气具有氧化性,用浓氨水检验Cl2管道是否泄漏 | |
| B. | 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 | |
| C. | 常温下浓硫酸与铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 | |
| D. | 钠的金属性比钾强,工业上用钠制取钾(Na+KCl$\frac{\underline{\;850℃\;}}{\;}$ K↑+NaCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属钠投入水中,浮在水面熔成小球,并在水面快速移动,得到的溶液显碱性;2 Na+2 H2O═2 NaOH+H2↑ | |
| B. | 氢气在氯气中安静的燃烧,发出淡蓝色火焰,瓶口出现白雾;H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | |
| C. | FeSO4溶液中加入NaOH溶液时,生成的白色絮状沉淀迅速变为灰绿色,最后变成红褐色; 2Fe(OH)2+O2+H2O═2 Fe(OH)3 | |
| D. | 向Na2SiO3溶液中逐滴加入稀盐酸,边加边振荡,有透明的硅酸凝胶产生;Na2SiO3+2HCl═H2SiO3(胶体)+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com