
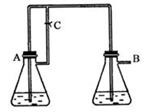
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
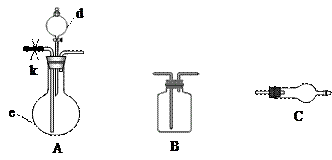
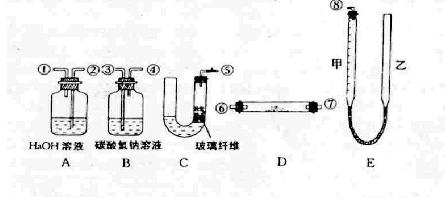
| 各装置连接次序 | | A | | | C | C |
| 对应的药品 | | d:浓盐酸 e:固体混合物 | | | 碱石灰 | 碱石灰 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
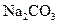 溶液除去
溶液除去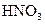 ,微热会产生黄色物质
,微热会产生黄色物质| A.①②③④ | B.②④⑤⑥ | C.①③⑤⑥ | D.①②③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.过滤 | B.蒸发 | C.分液 | D.萃取 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述实验证明了氧化性:Fe3+>Fe2+>Cu2+ |
| B.上述实验证明了Fe2+既有氧化性又有还原性 |
| C.实验①、③中的化学反应都是置换反应 |
| D.向三个实验后的溶液中加入足量NaOH溶液,最终都有Fe(OH)3生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油分馏时把温度计插入液面下 |
| B.向银氨溶液中加入几滴乙醛后用酒精灯加热至沸制银镜 |
| C.在试管内加入少量蔗糖溶液,再加3-5mL稀硫酸小心煮沸几分钟后冷却,加入新制Cu(OH)2悬浊液,煮沸,有红色沉淀生成 |
| D.用乙醇、醋酸和18mol/L的硫酸混合加热制乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com