
| A. | 原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似 | |
| B. | Zn2+核外电子排布式为1s22s22p63s23p63d10 | |
| C. | 基态铜原子的外围电子排布图: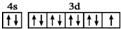 | |
| D. | 基态碳原子的最外层电子排布图: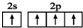 |
分析 A.1s2是He元素属于0族元素,1s22s2是Be元素属于第IIA族元素;
B.锌是30号,失去最外层2个电子得到锌离子,根据构造原理书写;
C.Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1,3d、4s能级上电子为其外围电子,然后确定外围电子排布图;
D.基态碳原子的核外电子排布式为1s22s22p2,最外层2s能级上是2个电子.
解答 解:A.1s2是He元素属于0族元素,1s22s2是Be元素属于第IIA族元素,二者性质不同,故A错误;
B.锌原子核外电子排布式为:1s22s22p63s23p63d104s2,失去最外层4s能级2个电子形成Zn2+,最外层已没有电子,故B正确;
C.Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1,3d能级上有10个电子、4s能级上有1个电子,3d、4s能级上电子为其外围电子,根据构造原理知其基态原子外围电子排布式为:3d104s1,图示中3d能级不是10个电子,故C错误;
D.基态碳原子的核外电子排布式为1s22s22p2,最外层2s能级上是2个电子,图示中是2s能级有1个电子跃迁到了2p能级的轨道上,故D错误;
故选B.
点评 本题考查了基态原子或离子的核外电子排布式、电子排布图,注意电子处于全满、半满、全空时最稳定,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.03mol/L | B. | 0.3mol/L | C. | 0.015mol | D. | 0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 步骤Ⅱ中无色气体是NO气体,无CO2气体产生 | |
| C. | 原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- | |
| D. | 为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L | B. | 0.5mol/L | C. | 0.045mol/L | D. | 0.45mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
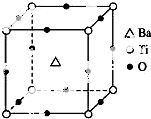 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )| A. | 8 BaTi8O12 | B. | 8 BaTi4O9 | C. | 6 BaTiO3 | D. | 3 BaTi2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 最高价都为+7 | B. | 从上到下原子半径逐渐减小 | ||
| C. | 从上到下非金属性逐渐减弱 | D. | 从上到下氢化物的稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
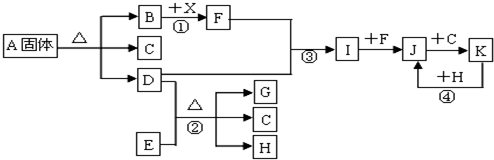
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
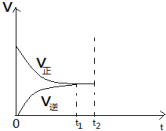 合成氨的反应中,在第一次平衡(t1时刻)后,在保持容器体积不变的情况下,在t2时刻及时分离出产物NH3,则此时平衡移动的情况是怎样的?请在图中将图补充完整.
合成氨的反应中,在第一次平衡(t1时刻)后,在保持容器体积不变的情况下,在t2时刻及时分离出产物NH3,则此时平衡移动的情况是怎样的?请在图中将图补充完整.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com