
 (NH4)2 SO4溶液中逐滴加入0.2000 mol
(NH4)2 SO4溶液中逐滴加入0.2000 mol NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42)>c(NH3·H2O )>c(OH-)>c(NH4+) |
科目:高中化学 来源:不详 题型:单选题
| A.水可以电离出离子,所以是强电解质 |
| B.水的离子积可表示KW=c(H+)·c(OH-) |
| C.常温下水中的c(H+)大于c(OH-) |
| D.升高温度,c(H+)增大,显弱酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在温度不变时,水溶液中c(H+)和c(OH-)不能同时增大 |
| B.pH=0的溶液是酸性最强的溶液 |
| C.强酸的水溶液中不存在OH- |
| D.某温度下,纯水中c(H+)=2×10-7mol·L-1,其呈酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.y=2ax+b | B.y=ax/(2x+3a) | C.a/2y-3a/2x=1 | D.x=2ay/(a+y) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ): n(
): n( )变化的关系如下表:
)变化的关系如下表:n( ): n( ): n( ) ) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
 )> c (
)> c ( ) > c (OH-) > c(H+)
) > c (OH-) > c(H+)  ) > c (
) > c ( ) > c (OH-) = c(H+)
) > c (OH-) = c(H+)  )+c (
)+c ( )
)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有(1) | B.只有(2) | C.(2)(3) | D.(1)(2)(3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知a g乙烯气体充分燃烧时生成1 mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH=-4b kJ·mol-1 |
B.将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+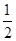 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1 |
| C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1 |
D.葡萄糖的燃烧热是2800kJ·mol-1,则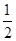 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400kJ·mol-1 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com