
下列电离方程式书写错误的是( )
A.CaCl2=Ca2++2Cl— B.H2CO3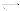 H++HCO3-
H++HCO3-
C.NaHCO3=Na++H++CO32- D.NaClO=Na++Cl O—
科目:高中化学 来源:2016届浙江省高一下学期期中考试化学试卷(解析版) 题型:选择题
将一定量的锌与100mL18.5mol/L浓硫酸充分反应,锌完全溶解,同时生成16.8L气体 (标准状况),将反应后的溶液稀释到1L,测得溶液的c(H+)=1mol/L,则下列叙述中错误的是
A.气体A为二氧化硫和氢气的混合物
B.气体A中二氧化硫和氢气的体积比为4:1
C.反应中共消耗锌95.5g
D.反应中共转移电子1.5mol
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
A.Na2O2只作氧化剂
B.Na2FeO4既是氧化产物又是还原产物
C.O2是还原产物
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.标准状况下,22.4L水中所含的分子数约为6.02×1023个
B.1 mol Cl2参加反应转移电子数一定为2 NA
C.标准状况下,aL氧气和氮气的混合物含有的分子数约为 ×6.02×1023个
×6.02×1023个
D.从1 L 0.5 mol/LNaCl溶液中取出100 mL,,剩余溶液中NaCl物质的量浓度为0.45mol/L
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列变化过程中不能直接实现的是( )
①HCl ②Cl2 ③Ca(ClO)2 ④HClO ⑤CO2
A.④→⑤ B.①→② C.③→④ D.②→③
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
有X、Y、Z、W四种元素,它们的单质X、Y、Z在常温常压下皆为气体,W为固体。
①X单质可在Z单质中燃烧生成XZ,其火焰为苍白色;W单质在Y单质中剧烈燃烧产生黄色火焰,生成W2Y2;
②每2molX2可与1molY2化合生成2molX2Y,X2Y在常温下为液体;
③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红色;
④Z单质溶于化合物X2Y,所得溶液具有漂白作用;请回答:
(1)画出Z原子的原子结构示意图 ;实验室中的W应保存在____________中(填试剂名称)
(2)写出化学式W2Y2___________ _ K#S5U
(3)写出与W+具有相同核外电子数的分子或原子,请写出任意3种的化学式
① ② ③
(4)Z单质与水反应的离子方程式:_________________________
⑸W单质与X2Y化学反应方程式:__________________________
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各组中的两种物质相互反应时,若改变反应条件(包括温度、反应物浓度、反应物用量比等),化学反应原理不改变的是
A.Na和O2 B.NaOH和CO2 C.NaHCO3与盐酸 D.MnO2与盐酸
查看答案和解析>>
科目:高中化学 来源:2016届浙江省湖州市高一上学期期末考试化学试卷(解析版) 题型:选择题
Na、Mg、Al三种金属各2mol分别跟1L1mol?L-1的盐酸反应时,相同条件下放出氢气体积最大的是
A.Al B. Mg C. Na D.三者产生的氢气一样多
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高一上学期期末模拟考试化学试卷(解析版) 题型:填空题
Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

已知NaHCO3在低温下溶解度较小。
反应Ⅰ:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl,处理母液的两种方法:
NaHCO3↓+NH4Cl,处理母液的两种方法:
(1)向母液中加入石灰乳,可将其中________循环利用。
(2)向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式 ___________。
Ⅱ.某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3。

(1)装置丙中冷水的作用是 ;
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有_______、洗涤、灼烧。NaHCO3转化为Na2CO3的化学方程式为 ;
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如图所示。

则曲线a对应的溶液中的离子是___________(填离子符号下同);曲线c对应的溶液中的离子是___________;该样品中NaHCO3和Na2CO3的物质的量之比是 ; 21
(4)若取21.0 g NaHCO3固体,加热了t2 rnin后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol?L—1的盐酸中,则充分反应后溶液中H+ 的物质的量浓度为____________(设溶液体积变化忽略不计)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com