
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是
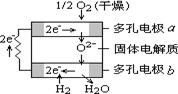
A.有O2放电的a极为电池的负极
B.有H2放电的b极为电池的正极
C.a极对应的电极反应为:O2 + 2H2O + 4e- = 4OH-
D.该电池的总反应方程式为:2H2 + O2 =2H2O
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
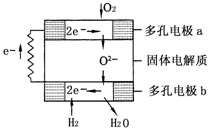 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:

A.有O2参加反应的a极为电池的负极
B.b极的电极反应为:H2-2e-+O2-====H2O
C.a极的电极反应为:O2+2H2O+4e-====4OH-
D.该电池的总反应式为:2H2+O2![]() 2H2O
2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
固体氧化物燃料电池是以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O 2-)在其间通过,该电池的工作原理如下图所示,其中多孔电极a\,b均不参与电极反应。下列判断正确的是
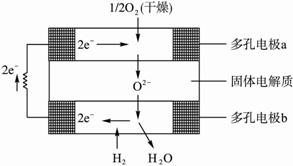
A. 有O2参加反应的a极为电池的负极
B. b极的电极反应为:H2-2e -+O 2-H2O
C. a极的电极反应为:O2+2H2O+4e -4OH -
D. 该电池的总反应式为:2H2+O2![]() 2H2O
2H2O
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省信阳高中高一下学期期中考试化学试卷(带解析) 题型:填空题
(9分)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如下表所示:
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 化学式 | A2C | A2C2 | D2C2 | D2E |

查看答案和解析>>
科目:高中化学 来源:2013届江西省高二第三次月考化学试卷 题型:选择题
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2- )在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是

A.有O2参加反应的a极为电池的负极
B.有H2参加反应的b极为电池的正极
C.a极对应的电极反应式为O2+2H2O-4e=4OH-
D.该电池的总反应方程式为:2H2+O2=2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com