
【题目】SO2和NOx都是大气污染物。
(1)汽车排放的尾气中含CO和NO,汽车发动机工作时产生的NO和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是_________________________________________;
(2)采取还原法,用炭粉可将氮氧化物还原.
已知:N2(g)+O2(g)=2NO(g)△H=+180.6kJmol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJmol-1
则反应C(s)+2NO(g)=CO2(g)+N2(g)△H=__________kJmol-1.
(3)将NO2变成无害的N2要找到适合的物质G与适当的反应条件,G应为_____________(填写“氧化剂”
或“还原剂”).下式中X必须为无污染的物质,系数n可以为0;
NO2+G![]() N2+H2O+nX (未配平的反应式);
N2+H2O+nX (未配平的反应式);
下列化合物中,满足上述反应式中的G是________(填写字母);
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
(4)利用氨水可以将SO2和NO2吸收,原理如图1所示:NO2被吸收的离子方程式是______________;
(5)利用图2所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2.
①b极的电极反应式为__________________________;
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成.该反应离子方程式为__________________________。

【答案】(1)2CO+2NO![]() 2CO2+N2 (2)-574.1 (3)还原剂;ad (4)2NO2+4HSO3-=N2+4SO42-+4H+ (5)①2HSO3-+2H++2e-=S2O42-+2H2O ②4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O
2CO2+N2 (2)-574.1 (3)还原剂;ad (4)2NO2+4HSO3-=N2+4SO42-+4H+ (5)①2HSO3-+2H++2e-=S2O42-+2H2O ②4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O
【解析】
试题分析:(1)CO和NO2通过催化转化器将其转化为无污染的两种气体是氮气和二氧化碳,反应为2CO+2NO![]() 2CO2+N2;
2CO2+N2;
(2)根据盖斯定律,一个反应无论是一步完成还是分为几步完成,其热效应是相同的,已知:
N2(g)+O2(g)=2NO(g)△H=+180.6kJmol-1 ①
C(s)+O2(g)=CO2(g)△H=-393.5kJmol-1 ②
将②-①可得:C(s)+2NO(g)=CO2(g)+N2(g)△H=-393.5kJmol-1-180.6kJmol-1=-574.1KJ/mol;
(3)将NO2变成无害的N2中,氮元素的化合价降低了,二氧化氮做氧化剂,需要加入还原剂,在下列四种物质:a.NH3 b.CO2 c.SO2 d.CH3CH2OH中,能被二氧化氮氧化具有还原性的物质有乙醇和NH3;
(4)氨水可以将SO2和NO2同时吸收处理,二氧化硫与氨水反应生成亚硫酸氢根离子,NO2被吸收的离子方程式是2NO2+4HSO3-=N2+4SO42-+4H+;
(5)①依据图示可知,阴极上HSO3-得电子生成S2O42-,阴极区发生反应2HSO3-+2H++2e-=S2O42-+2H2O;
②阴极排出的溶液为S2O42-,二氧化氮与其发生反应,S2O42-中硫元素由+3价,变为硫酸根中硫元素为+4价,S2O42-被氧化是还原剂;二氧化氮中的氮元素化合价为+4价变为氮气0价,二氧化氮被还原为氧化剂,依据原子守恒和得失电子守恒可得,发生的离子方程式为4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子因发生氧化还原反应而不能大量共存的是( )
A.H+、Fe2+、NO3﹣、SO42﹣
B.Al3+、Na+、SO42﹣、HCO3﹣
C.Na+、Ca2+、Cl﹣、SO42﹣
D.Fe3+、K+、SCN﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验。请回答下列问题:
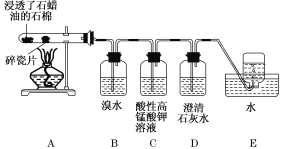
(1)A中碎瓷片的作用是 。
(2)B装置中反应的化学方程式为: 。
(3)C装置中可观察到的现象是__________________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填字母)中的实验现象可判断该资料是否真实。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________(选填字母,下同);除去甲烷中乙烯的方法是__________。
A.气体通入水中
B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
(6)下列物质中,不是通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验需要0.80 mol·L-1 NaOH溶液475 mL和0.40 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
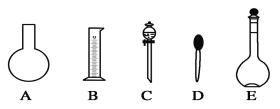
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)下列操作中,不能用容量瓶实现的有______________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为_______g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度______(填”大于”、“等于”或“小于”,下同)0.8 mol·L-1。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度______0.8 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、20 mL、50 mL量筒,选用________mL量筒最好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如右图所示。下列判断正确的是( )
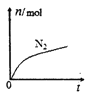
A.该反应的还原剂是Cl-
B.消耗lmol还原剂,转移6mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一些茶叶的包装盒中有一个小袋,将小袋打开可看到灰黑色粉末,其中有的已变成棕褐色。将这种灰黑色粉末投入稀盐酸后,取其上层清液并加几滴氯水,再滴加KSCN溶液,马上出现红色。以下结论不正确的是 ( )
A.该灰黑色粉末作抗氧化剂
B.该灰黑色粉末不可食用
C.小袋中原来装有铁粉
D.小袋中原来装有氧化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用量筒量取液体时,将量筒平放,仰视液体凹液面最低处读数为16.0 mL,倾倒出一部分溶液,又俯视液体凹液面最低处,读数为10.0 mL,该同学取出液体的体积是()
A. 大于6.0 mL B. 等于6.0 mL
C. 小于6.0 mL D. 无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com