
 2C(g) ��2D(g)��2 min ĩ��Ӧ�ﵽƽ��״̬������0.8 mol D������д����հף�
2C(g) ��2D(g)��2 min ĩ��Ӧ�ﵽƽ��״̬������0.8 mol D������д����հף�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 NO2��CO ������˵����ȷ���ǣ� ��
NO2��CO ������˵����ȷ���ǣ� ��| A�������¶ȣ�����Ӧ���������淴Ӧ���ʼ��� |
| B������ʱ��ѹ���������������ɫ�����ƽ������ |
C���ﵽƽ�⣬��ƽ�ⳣ��Ϊ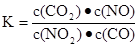 |
| D������ʱ�������¶ȣ�����������ɫ����÷�Ӧ���ʱ�Ϊ��ֵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)��D(g)���������������������仯ʱ���ٻ��������ܶȢ������������ѹǿ�ۻ�������ƽ����Է���������B�����ʵ���Ũ�� �ܱ����÷�Ӧһ���Ѵﵽƽ��״̬���ǣ� ��
C(g)��D(g)���������������������仯ʱ���ٻ��������ܶȢ������������ѹǿ�ۻ�������ƽ����Է���������B�����ʵ���Ũ�� �ܱ����÷�Ӧһ���Ѵﵽƽ��״̬���ǣ� ��| A���٢ۢ� | B���ڢ� | C���ڢۢ� | D��ֻ�Т� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
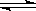 3KCl + Fe(SCN)3���ﵽƽ�����Һ�Ժ�ɫ����ʹƽ�������ƶ���������
3KCl + Fe(SCN)3���ﵽƽ�����Һ�Ժ�ɫ����ʹƽ�������ƶ���������| A������Һ�м�����KCl���� | B������Һ�м�������ˮ |
| C������Һ�е������� 1mol/L FeCl3 | D���跨���߲���ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
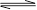 2NO��O2���˷�Ӧ�ﵽƽ��״̬ʱ�ı�־��(����)
2NO��O2���˷�Ӧ�ﵽƽ��״̬ʱ�ı�־��(����)| A������������ɫ��dz |
| B�����������ܶȲ��ٱ仯 |
| C���������NO2��NO��O2���ʵ���֮��Ϊ2��2��1 |
| D����λʱ��������2n mol NO��ͬʱ����2n mol NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������8 mol | B������1.6 mol | C������0.8 mol��1.6 mol? | D������1.6 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
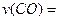 ��
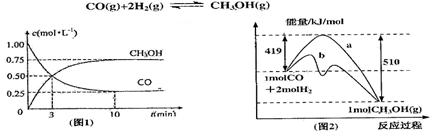
��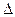 H>0������Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȣ�
H>0������Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȣ� ��ʽΪ ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������
��ʽΪ ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������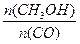 ����� ��
����� �� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
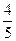 ,��N2��ת����Ϊ
,��N2��ת����Ϊ| A��50% | B��37.5% | C��25% | D��12.5% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
 2SO3(g)
2SO3(g)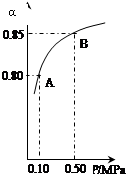
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/mol��L��1 | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com