
| A. | 常温常压下,35.5g的氯气与足量的氢氧化钙溶液完全反应,转移的电子数为0.5NA | |
| B. | 60g甲酸甲酯和葡萄糖的混合物含有的碳原子数目为2NA | |
| C. | 标准状况下,2.24L PH3与3.4gH2S气体分子所含电子数目均为1.8NA | |
| D. | 已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,当该反应生成NA个NH3分子时,反应放出的热量小于46.2kJ |
分析 A、求出氯气的物质的量,然后根据氯气和碱的反应为歧化反应来分析;
B、甲酸甲酯和葡萄糖的最简式均为CH2O;
C、求出PH3和H2S的物质的量,然后根据PH3和H2S中均含18个电子来分析;
D、合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol的含义是当1mol氮气和3mol氢气反应生成2mol氨气时,放出92.4KJ的热量.
解答 解:A、35.5g氯气的物质的量为0.5mol,而氯气和碱的反应为歧化反应,1mol氯气转移1mol电子,故0.5mol氯气转移0.5NA个电子,故A正确;
B、甲酸甲酯和葡萄糖的最简式均为CH2O,故60g甲酸甲酯和葡萄糖的混合物中含有CH2O的物质的量为2mol,故含2NA个碳原子,故B正确;
C、标况下2.24LPH3和3.4gH2S的物质的量均为0.1mol,而PH3和H2S中均含18个电子,故0.1molPH3和0.1molH2S中含有的电子均为1.8NA个,故C正确;
D、合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol的含义是当1mol氮气和3mol氢气反应生成2mol氨气时,放出92.4KJ的热量,故当生成NA个氨气分子时,放出46.2KJ热量,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构


科目:高中化学 来源: 题型:实验题
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol•L-1 NaOH溶液 | 50 mL 0.5 mol•L-1 HCl溶液 | 20℃ | 23.3℃ | -56.8kJ/mol |
| ② | 50 mL 0.55 mol•L-1 NaOH溶液 | 50 mL 0.5 mol•L-1 HCl溶液 | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散系的分类: 分散系微粒直径 分散系微粒直径 | |
| B. | 溶液是电中性的,而胶体是带电的 | |
| C. | 光线通过时,溶液产生丁达尔效应,胶体则无丁达尔效应 | |
| D. | 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓HNO3能与碳反应,说明其具有强氧化性 | |
| B. | 浓HNO3能溶解金属铜,说明其具有强酸性 | |
| C. | 浓HNO3不稳定易分解,需要避光保存 | |
| D. | 常温下浓HNO3能使金属铝钝化,可以用铝槽车运输浓HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯氏制碱法制得的是纯碱 | |
| B. | 用人参泡制药酒是利用了萃取的原理 | |
| C. | 氢氟酸刻蚀玻璃是利用了氢氟酸的强氧化性 | |
| D. | 硫酸铜溶液可用于特定环境中的消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
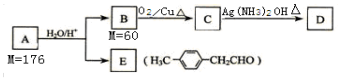
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
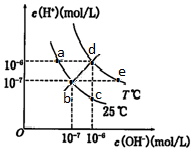
| A. | c点对应的溶液中大量存在的离子可能为:NH4+、Ba2+、Cl-、I- | |
| B. | a点对应的溶液中水的电离程度可能大于c点对应的溶液中水的电离程度 | |
| C. | 将25℃时的NaCl溶液加热到T℃,则该溶液中的c(OH-)由b点变化到e点 | |
| D. | bd线上的任意一点均有pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ②⑤⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤所需实验用品有漏斗、烧杯、玻璃棒、铁架台(带铁圈) | |
| B. | 过滤时把漏斗放在铁三脚架上 | |
| C. | 过滤时将玻璃棒斜靠在三层滤纸上 | |
| D. | 过滤时为了加快过滤速度,用玻璃棒搅拌过滤器中的液体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com