
分析 (1)碘离子具有还原性,能被空气中的氧气氧化为碘单质,根据电子守恒来配平方程式即可;
(2)化合价降低元素对应的产物是还原产物;
(3)根据化学方程式结合电子转移进行计算即可.
解答 解:(1)碘离子具有还原性,能被空气中的氧气氧化为碘单质,化合价升高的元素是I元素,化合价降低的是氧元素,化合价升高值=化合价降低值=转移电子数=4,所以碘化钾前边系数是4,氧气的前边系数是1,电子转移如下: ,故答案为:
,故答案为: ;
;
(2)化合价降低的氧元素对应的产物KOH是还原产物,故答案为:KOH;
(3)当有4mol电子发生转移时,生成I2的物质的量是2mol,有0.2mol电子发生转移时,生成I2的物质的量是0.1mol,质量是0.1mol×254g/mol=25.4g,故答案为:25.4g.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素化合价变化为解答的关键,注意分析反应中元素的化合价,侧重氧化还原反应基本概念的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2(g)+Cl2(g)=$\frac{1}{2}$HCl(g)△H=92.4KJ/mol | B. | H2(g)+Cl2(g)=$\frac{1}{2}$HCl(g)△H=-92.4KJ/mol | ||
| C. | H2(g)+Cl2(g)=2HCl(g)△H=-184.8KJ/mol | D. | H2(g)+Cl2(g)=2HCl(l)△H=184.8/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某品牌食品调料标签的一部分如图.
某品牌食品调料标签的一部分如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
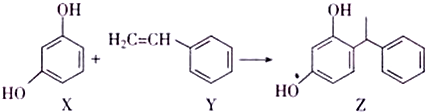
| A. | X、Y和Z均能使溴水褪色,且原理相同 | |
| B. | X和Z均能与Na2CO3溶液反应放出CO2 | |
| C. | Z中含手性碳原子 | |
| D. | Y可作加聚反应的单体,X可作缩聚反应的单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 叙述 | 判断 |
| A | 1molH2O | 标准状况下,其体积约为22.4L | 正确 |
| B | 2gH2 | 常温常压下,有NA个氢分子 | 错误 |
| C | 1L0.1mol?L-1NaCl溶液 | 取出100mL,NaCl的物质的量浓度为0.1mol?L-1 | 正确 |
| D | 1mol?L-1Na2SO4溶液 | 将1molNa2SO4固体溶于1L水可配得该溶液 | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
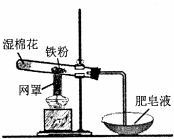
| A. | 该反应属于复分解反应 | |
| B. | 网罩的作用是集中火焰,提高温度 | |
| C. | 湿棉花的作用是给试管降温,防止炸裂 | |
| D. | 反应中水既不是氧化剂,也不是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com