
【题目】在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)![]() CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )

A.平衡常数K=![]()
B.该反应在T1时的平衡常数比T2时的小
C.CO合成甲醇的反应为吸热反应
D.处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
【答案】D
【解析】
A.CO(g)+2H2(g)CH3OH(g)的平衡常数表达式K=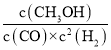 ,故A错误;
,故A错误;
B.由图可知,T2温度下到达平衡需要的时间较短,反应速率较快,故温度T2>T1。温度越高,平衡时甲醇的物质的量越小,说明升高温度平衡向逆反应方向移动,化学平衡常数减小,在T1时的平衡常数比T2时的大,故B错误;
C.由图可知,T2温度下到达平衡需要的时间较短,反应速率较快,故温度T2>T1。温度越高,平衡时甲醇的物质的量越小,说明升高温度平衡向逆反应方向移动,所以合成甲醇的反应为放热反应,故C错误;
D.由图可知,处于A点的反应体系从T1变到T2,温度升高,平衡向逆反应方向移动,氢气物质的量增大,甲醇的物质的量减小,![]() 增大,故D正确;
增大,故D正确;
故选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其周期数相同;B的价电子排布式为nsnnpn+2;短周期元素C和D为同周期不相邻的元素,C是同周期元素中离子半径最小的元素,D元素最外层有两个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ECl4(氯化物)溶液的方法制备纳米材料。回答下列问题:
(1)D元素在周期表中的位置为__________________,E原子核外有_____个未成对电子,五种元素中电负性最大的是___________(填元素名称)。
(2)由A、B、D三种元素形成的常见三元化合物中具有强氧化性的是______(填化学式)。
(3)A、B、D元素形成的化合物有A2B、DB3,下列关于A2B和DB3的说法中,正确的是______(填标号)。
A.中心原子的价层电子对数目相等B.都是非极性分子C.中心原子的孤电子对数目相等D.都含有极性键E.都能与Na2O反应F.固态时晶体类型不同
(4)D在空气中燃烧的产物分子构型为______。固体DB3中存在如图(b)所示的三聚分子,该分子中D原子的杂化轨道类型为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量![]() ,较多的
,较多的![]() 及部分污泥,通过下列流程可从该废水中回收
及部分污泥,通过下列流程可从该废水中回收![]() 晶体及金属Cu。
晶体及金属Cu。

![]() 固体混合物是______
固体混合物是______![]() 填化学式
填化学式![]() ,试剂乙为______
,试剂乙为______![]() 填物质名称
填物质名称![]()
![]() 步骤3中发生反应的离子方程式为______
步骤3中发生反应的离子方程式为______
![]() 步骤4中涉及的操作是:蒸发浓缩、______、过滤、洗涤、干燥;蒸发浓缩、过滤操作中均用到的玻璃仪器是______
步骤4中涉及的操作是:蒸发浓缩、______、过滤、洗涤、干燥;蒸发浓缩、过滤操作中均用到的玻璃仪器是______
![]() 粗铜中常混有少量氧化亚铜
粗铜中常混有少量氧化亚铜![]() ,氧化亚铜与稀硫酸反应,会产生单质铜,同时溶液变蓝。试写出该反应的离子方程式______。
,氧化亚铜与稀硫酸反应,会产生单质铜,同时溶液变蓝。试写出该反应的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加徳罗常数的值,下列说法正确的是
A. 常温下,1L pH=13的Ba(OH)2溶液中OH-数为0.2NA
B. 2.4g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA
C. 氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA
D. 0.lmol/L(NH4)2SO4溶液与0.2mol/LNH4Cl溶液中的NH4+数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下,某恒容容器中发生反应SO2(g)+NO2(g)![]() SO3(g)+NO(g),其平衡常数K=0.24,下列说法正确的是
SO3(g)+NO(g),其平衡常数K=0.24,下列说法正确的是
A.该温度下反应2SO2(g)+2NO2(g)![]() 2SO3(g)+2NO(g)的平衡常数为0.48
2SO3(g)+2NO(g)的平衡常数为0.48
B.若该反应ΔH<0,则升高温度化学平衡常数K减小
C.若升高温度,逆反应速率减小
D.改变条件使平衡正向移动,则平衡时容器中![]() 一定比原平衡小
一定比原平衡小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2 mol SO2和1mol O2,乙中充入4 mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)![]() 2SO2(g)+ O2(g)。下列有关说法正确的是
2SO2(g)+ O2(g)。下列有关说法正确的是
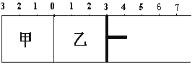
A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强:P乙=P甲
B.若活塞固定在3处不动,达平衡时甲乙两容器中SO3的浓度: c(SO3)乙>2c(SO3)甲
C.若活塞固定在3处不动,达平衡时甲乙容两器中SO2的体积分数:ψ(SO2)乙>2ψ(SO2)甲
D.若活塞固定在7处不动,达平衡时两容器中SO3的物质的量分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中充入2molA和1molB,发生反应:2A(气)+B(气) ![]() xC(气),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质,达到平衡后,C的体积分数仍为W%,则x值为
xC(气),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质,达到平衡后,C的体积分数仍为W%,则x值为
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子或分子在溶液中能大量共存,且满足相应要求的是( )
选项 | 离子或分子 | 要求 |
A | K+、SO | c(K+)=2c(SO |
B | Fe3+、Na+、NO | 溶液pH=1 |
C | NH | 滴加NaOH溶液马上有气泡产生 |
D | Na+、Al3+、Cl-、SO | 滴加氨水立即有沉淀产生 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.114号元素在周期表中第七周期第VIA族,属于金属元素
B.晶体硅熔点高硬度大,可用于制作光导纤维
C.为了除去MgCl2酸性溶液中的Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入MgCO3,过滤后,再向滤液中加入适量的盐酸
D.光束通过下列分散系①有尘埃的空气②明矾溶液③墨水④稀豆浆时,都能产生丁达尔效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com