
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3-OH- Cl- |

分析 ①将它们溶于水后,D为蓝色溶液,其他均为无色溶液,则D中含有铜离子;
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解,则C中含有铝离子,E中含有氢氧根离子;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃),则B中含有钾离子,其它金属离子与氢氧根离子不能共存,所以E是氢氧化钠;
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,则A中含有碳酸氢根离子,D中产生白色沉淀,则D中含硫酸根离子,所以D是硫酸铜;
⑤将B、C两溶液混合,未见沉淀或气体生成,则B是氯化钾,C为氯化铝,所以A是碳酸氢钠
综上可知,A为NaHCO3,B为KCl,C为AlCl3,D为CuSO4,E为NaOH,以此来解答.
解答 解:①将它们溶于水后,D为蓝色溶液,其他均为无色溶液,则D中含有铜离子;
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解,则C中含有铝离子,E中含有氢氧根离子;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃),则B中含有钾离子,其它金属离子与氢氧根离子不能共存,所以E是氢氧化钠;
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,则A中含有碳酸氢根离子,D中产生白色沉淀,则D中含硫酸根离子,所以D是硫酸铜;
⑤将B、C两溶液混合,未见沉淀或气体生成,则B是氯化钾,C为氯化铝,所以A是碳酸氢钠
综上可知,A为NaHCO3,B为KCl,C为AlCl3,D为CuSO4,E为NaOH,
(1)B、D的化学式分别为K2SO4、CuSO4,故答案为:KCl;CuSO4;
(2)C为AlCl3可用作净水剂,在溶液中铝离子水解生成氢氧化铝胶体,能净水,其水解离子方程式:Al3++3H2O═Al(OH)3+3H+;
故答案为:Al3++3H2O═Al(OH)3+3H+;
(3)将含0.01molNaHCO3的溶液与含0.02mol NaOH的溶液反应生成0.01molNa2CO3,还剩余0.01molNaOH,向溶液中滴加0.1mol•L-1稀盐酸,先与NaOH反应,然后与Na2CO3反应生成NaHCO3,再与NaHCO3反应生成二氧化碳气体,三个反应中消耗的HCl相同,所以前面消耗0.2LHCl时,没有气体生成,最后消耗0.1LHCl生成气体,C项符合;
故答案为:C;
(4)在mmL bmol•L-1 AlCl3溶液中,加入等体积a mol•L-1的NaOH溶液.当a≤3b时,氢氧化钠不足,则按照NaOH计算,则氢氧化铝的物质的量为$\frac{1}{3}$×m×a×10-3=$\frac{am}{3000}$mol;
当3b<a<4b件时,发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,
生成沉淀的物质的量等于bm×10-3-(am×10-3-3bm×10-3)mol=(4bm-am)×10-3mol;
故答案为:$\frac{am}{3000}$;(4bm-am)×10-3.
点评 本题考查无机物的推断、离子反应和离子鉴别,把握离子之间的反应推断物质为解答的关键,侧重分析、推断能力和计算能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 熔点:CO2<H2O<SiO2<KCl | B. | 稳定性:H2O<NH3<PH3<SiH4 | ||
| C. | 酸性:H3PO4>H2SO4>HClO4>H2SiO3 | D. | 粒子半径:K+>Na+>Mg2+>Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
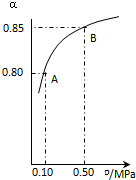 二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:4 | B. | 4:5 | C. | 2:1 | D. | 4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| C. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | CaCO3溶于稀盐酸中:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NF3是氧化剂,H2O是还原剂 | |
| B. | 还原剂与氧化剂的物质的量之比为2:1 | |
| C. | 若生成0.2mol HNO3,则转移0.2mol电子 | |
| D. | NF3气体应密封干燥保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定存在的离子是Na+、SO32-、NO3-、AlO2- | |
| B. | 一定存在的离子是Na+、SO32-、CO32-、AlO2- | |
| C. | 可能存在的离子是Al3+、CO32- | |
| D. | 可能存在的离子是CO32-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 反应物 | 产物 |
| ① | Cl2、H2O2 | Cl- |
| ② | Cl2、FeI2 | FeCl2、I2 |
| ③ | KClO3、HCl | Cl2、KCl、H2O |
| A. | 第①组反应的氧化产物为O2 | |
| B. | 第②组反应中Cl2 和FeI2的物质的量之比小于或等于1:1 | |
| C. | 第③组反应中生成1molCl2转移6mol电子 | |
| D. | 氧化性由强到弱的顺序为ClO3->Cl2>I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com