
【题目】合成氨工业对化学工业和国防工业具有重要意义,对农业生产起着重要作用。
(1)已知:N2(g)+O2(g)=2NO(g) △H1
H2(g)+1/2O2(g)=H2O(1) △H2
4NH3(g)+5O2(g)=4NO(g)+6H2O(1) △H3
N2(g)+3H2(g)2NH3(g) △H4<0
则△H4= (用含△H1、△H2、△H3的代数式表示)。
(2)在其他条件相同时,分别测定合成氨反应中N2的平衡转化率随压强变化的曲线如下图A、B所示,其中正确的是 (填“A”或“B”),其判断理由是 。
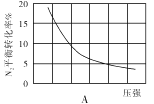
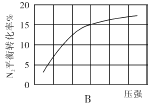
(3)在体积为2L的密闭容器中按物质的量1:3的比例充入N2、H2,进行下列四组合成氨实验:
组别 | 温度 | N2起始量/mol | N2的物质的量/mol | ||||||
5(s) | 10(s) | 15(s) | 20(s) | 25(s) | 30(s) | 35(s) | |||
Ⅰ | T1 | 0.1 | 0.094 | 0.089 | 0.085 | 0.0825 | 0.081 | 0.080 | 0.080 |
Ⅱ | T2 | 0.1 | 0.090 | 0.085 | 0.082 | 0.080 | 0.080 | 0.080 | 0.080 |
Ⅲ | T3 | 0.2 | 0.179 | 0.165 | 0.153 | 0.146 | x | x | x |
Ⅳ | T4 | 0.2 | 0.173 | 0.161 | 0.155 | 0.150 | 0.150 | 0.150 | 0.150 |
①实验Ⅰ前10秒的平均速率v(NH3)= mol·L-1·s-1,T1温度下合成氨反应的平衡常数K= (列出计算式)。
②与实验Ⅰ相比,实验Ⅱ改变了一个条件,该条件可能是 。
③与实验I相比,实验Ⅲ中N2的平衡转化率 (填“增大”、“减小”或“不变”),平衡常数K (填“增大”、“减小”或“不变”)。
④实验Ⅲ与实验Ⅳ的反应条件温度不同,则T1 (填“大于”、“小于”或“等于”)T2,原因是 。
【答案】(1)△H1+3△H2-1/2△H3
(2)B;合成氨反应为气体分子数减小的反应,增大压强,平衡正移,反应物的转化率增大
(3)①0.0011 ![]() (mol·L-1)-2[答出5.79 (mol·L-1)-2也可]
(mol·L-1)-2[答出5.79 (mol·L-1)-2也可]
②加催化剂 ③增大 不变
④小于 T2时的平衡常数小于T1时的平衡常数且正反应放热(或Ⅳ中前10s的平均反应速率比Ⅲ大,N2的平衡转化率比Ⅲ小)
【解析】
试题分析:(1)已知:①N2(g)+O2(g)=2NO(g) △H1
②H2(g)+1/2O2(g)=H2O(1) △H2
③4NH3(g)+5O2(g)=4NO(g)+6H2O(1) △H3
则根据盖斯定律可知①+3×②-0.5×③即得到N2(g)+3H2(g)![]() 2NH3(g)的反应热△H4=△H1+3△H2-1/2△H3。
2NH3(g)的反应热△H4=△H1+3△H2-1/2△H3。
(2)合成氨反应是体积减小的可逆反应,增大压强平衡向正反应方向进行,氮气的转化率增大,则装置图B正确。
(3)①实验Ⅰ前10秒内消耗氮气是0.1mol-0.089mol=0.011mol,则生成氨气是0.022mol,浓度是0.011mol/L,所以平均速率v(NH3)=0.011mol/L÷10s=0.0011mol·L-1·s-1;T1温度下平衡时消耗氮气是0.02mol,同时消耗氢气是0.06mol,生成氨气是0.04mol,则平衡时氮气是0.04mol/L,氢气是0.12mol/L,氨气是0.02mol/L,则合成氨反应的平衡常数K=![]() (mol·L-1)-2。
(mol·L-1)-2。
②与实验Ⅰ相比,实验Ⅱ到达平衡的时间减少,平衡状态不变,则改变的条件可能是使用了催化剂。
③实验Ⅲ中进行到20s时氮气的转化率是![]() ,实验I氮气的平衡转化率是0.2,所以与实验I相比,实验Ⅲ中N2的平衡转化率增大,温度不变,平衡常数K不变。
,实验I氮气的平衡转化率是0.2,所以与实验I相比,实验Ⅲ中N2的平衡转化率增大,温度不变,平衡常数K不变。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】注射用双黄连以绿原酸为主要成分(其结构如右图), 。绿原酸有广泛的药理作用。
。绿原酸有广泛的药理作用。
已知一个绿原酸分子在酸性条件水解得到一个咖啡酸A分子(环上有3个取代基)和一个奎尼酸分子,某小组对A的研究如下:

(1)咖啡酸A分子中含有的官能团为 (写名称);奎尼酸的结构简式为 ;
(2)反应①的反应类型为 ;
(3)反应②中1 mol B生成1mol C需NaOH的物质的量 ;
(4)写出A生成B的化学方程式 ;
(5)写出符合下列4个条件的A的所有同分异构体的结构简式 ;
①遇FeCl3溶液显色;
②1 mol E能消耗2 mol Na或1 mol NaOH;
③l mol E与足量新制Cu(OH)2反应生成2 mol Cu2O;
④苯环上只有一种化学环境的氢。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是( )
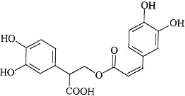
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和9mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
 D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
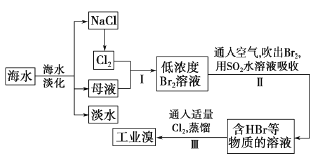
(1)请列举海水淡化的两种方法:________、_________。
(2)步骤I中己获得Br2,步骤II中又将Br2还原为Br-。其目的是_____。
(3)步骤II用SO2水溶液吸收Br2,吸收率可达95% 。有关反应的离子方程式为_________。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法。查阅了有关资料知:Br2的沸点为59 ℃.微溶于水,有毒并有强腐蚀性。他们参观生产过程后.画了如下装置简图:
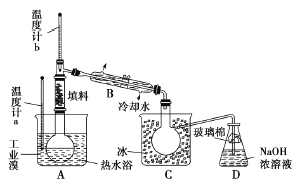
请你参与分析讨论:
①图中仪器B的名称是_______。
② 整套实验装皿中仪器连接均不能用橡胶塞和橡胶管。其原因是_______。
③ 实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?_______。
④ C中液体颜色为_______。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr,溶液,充分反应后.再进行的分离操作是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某+2价离子的电子排布式为1s22s22p43s23p43d10,该元素在周期表中所属的族是( )
A. ⅡA B. ⅡB C. ⅤⅡ D. ⅠB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学元素家族又添新成员,113号元素Uut和115号元素Uup。已知113号元素的一种核素为![]() Uut,下列说法中正确的是
Uut,下列说法中正确的是
A. 113号元素的相对原子质量为278
B. 115号元素可显+5价
C. ![]() Uut的中子数与电子数之差为165
Uut的中子数与电子数之差为165
D. 两种元素均位于周期表第八周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种气态烃,标况下的密度为1.25g/L,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
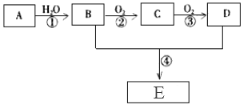
(1)写出A的结构简式 。
(2)B、D分子中所含官能团的名称分别是 、 。
(3)物质B可以直接氧化为D,需要加入的试剂是 。
(4)写出下列反应的化学方程式:
反应②的化学方程式: ;反应类型: 。
反应④的化学方程式: ;反应类型: 。
(5)B可由含淀粉的农产品如玉米、小麦、薯类等经发酵、蒸馏而得。请写出淀粉水解的化学方程式。
____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.配制硫酸亚铁溶液时,常向溶液加入少量稀硝酸和少量铁粉
B.用25.00mL碱式滴定管量取20.00mL酸性高锰酸钾溶液
C.用pH试纸检验气体的酸碱性时,一定要先用蒸馏水湿润
D.可以用洒精萃取碘水中的碘单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com