
用下列实验或实验装置进行的实验中,能达到相应实验目的的是( )
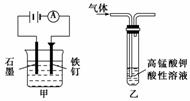
A.装置甲:防止铁钉生锈
B.测定同温同浓度的NaCl和NaF溶液的pH,确定F、Cl两元素的非金属性的强弱
C.装置乙:除去乙烷中混有的乙烯
D.用Ca(OH)2溶液来鉴别Na2CO3溶液和NaHCO3溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列中学常见实验的现象或表述正确的是 ( )。
A.过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加KSCN溶液,溶液显血红色
B.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可
D.向CuSO4溶液中滴入过量NaOH溶液充分反应后,将混合液体倒入蒸发皿中加热煮沸一会,然后冷却、过滤,滤纸上的物体为“蓝色固体”
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中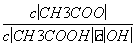 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组原子中,彼此化学性质一定相似的是( )
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y 原子
原子
D.最 外层都只有一个电子的X、Y原子
外层都只有一个电子的X、Y原子
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子的核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________周期第________族。W的气态氢化物稳定性比H2O(g)________(填“强”或“弱”)。
(2)Y的基态原子的核外电子排布式是________,Y的第一电离能比X的________(填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是__________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组同学以碳棒为电极电解CuCl2溶液时,发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,同学们设计了如下实验过程。
(1)对比实验(以碳棒为电极电解下列溶液)
| 电解质溶液 | 阴极析出物质 | |
| 实验1 | CuSO4溶液 | 红色固体 |
| 实验2 | CuSO4和NaCl的混合溶液 | 红色固体和少量白色固体 |
(2)提出假设
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为________。
(3)实验验证
取电解CuCl2溶液后的阴极碳棒,洗涤、干燥。连接下列装置进行实验,验证阴极产物。
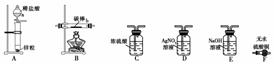
仪器a的名称为________,各装置从左至右的连接顺序为________。
(4)观察现象,得出结论
实验结束后,碳棒上的白色物质变为红色,F中物质不变色,D中出现白色沉淀。
根据现象写出装置B中发生反应的化学方程式:
________________________________________________________________________。
(5)问题讨论
①欲洗去碳棒上的红色和白色物质,可将碳棒插入稀硝酸中,则红色物质消失的离子方程式为______________________;白色物质消失的离子方程式为_________________
______________________。
②实验过程中,若装置B中的空气没有排净就开始加热,可能对实验造成的影响是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是
( )
A.Ba(OH)2、KSCN、NaCl、Mg(NO3)2(FeCl3溶液)
B.NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3(H2SO4溶液)
C.NH4Br、K2CO3、NaI、CaCl2(AgNO3溶液)
D.(NH4)3PO4、NaBr、CuSO4、AlCl3(KOH溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知具有碳碳双键结构的有机物可被碱性高锰酸钾溶液氧化成二元醇,如H2C===CH2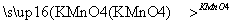 HOCH2CH2OH。现以CH2===C(CH3)2为原料按下列方式合成环状化合物D和高分子化合物G。
HOCH2CH2OH。现以CH2===C(CH3)2为原料按下列方式合成环状化合物D和高分子化合物G。
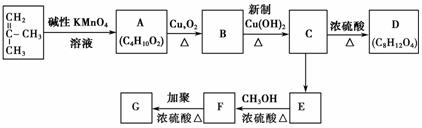
(1)A→B的反应类型是________,C→E的反应类型是________,E→F的反应类型是________。
(2)D的结构简式是________,G的结构简式是________。
(3)B→C的化学方程式是________________________________________________________________________。
(4)E→F的化学方程式是________________________________________________________________________。
(5)C物质的同分异构体中,与C所含官能团种类和数目都相同的同分异构体有________种(不包括C)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于反应Zn+2HNO3+NH4NO3===N2↑+3H2O+Zn(NO3)2,下列判断正确的是( )
A.生成1 mol N2,电子转移总数为3NA
B.生成1 mol N2,电子转移总数为5NA
C.溶解1 mol Zn,电子转移总数为2NA
D.溶解1 mol Zn,电子转移总数为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com