
【题目】环扁桃酯是用于治疗心脑血管疾病的重要化合物,它的一种合成路线如图. 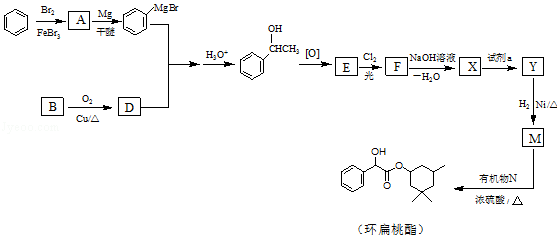
已知: 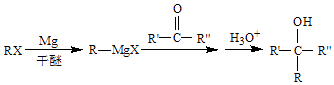 (R、R′、R″代表烃基或氢)
(R、R′、R″代表烃基或氢)
(1)A的结构简式是 .
(2)B→D的化学方程式是 .
(3)红外吸收光谱表明E有C=O键.F的分子式为C8H6Cl2O. ①E的结构简式是 .
②E→F的反应类型是 .
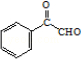
(4)X的结构简式是 .
(5)试剂a是 .
(6)生成环扁桃酯的化学方程式是 .
(7)以CH3CH=CH2、CH3CHO为有机原料,结合题目所给信息,选用必要的无机试剂合成CH2=CHCH=CHCH3 , 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
【答案】
(1)![]()
(2)2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
(3)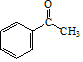 ;取代反应
;取代反应
(4)
(5)O2
(6)
(7)![]()
![]()
![]()
【解析】解: ![]() 与Br2在FeBr3作催化剂的条件下发生取代反应,故A的结构简式为
与Br2在FeBr3作催化剂的条件下发生取代反应,故A的结构简式为 ![]() ,B应该是醇在Cu作催化剂的条件下催化氧化生成D(醛),结合题目给的已知条件,以及产物
,B应该是醇在Cu作催化剂的条件下催化氧化生成D(醛),结合题目给的已知条件,以及产物 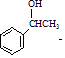 ,得到D的结构简式为CH3CHO,故B的结构简式为CH3CH2OH,
,得到D的结构简式为CH3CHO,故B的结构简式为CH3CH2OH,  2﹣羟基醇氧化生成酮,则E的结构简式为
2﹣羟基醇氧化生成酮,则E的结构简式为 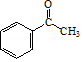 ,
, 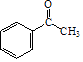 和Cl2在光照的条件下发生取代反应,且F的分子式为C8H6Cl2O,故F的结构简式为
和Cl2在光照的条件下发生取代反应,且F的分子式为C8H6Cl2O,故F的结构简式为 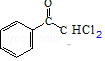 ,F和NaOH水溶液发生取代反应,得到的产物中一个碳原子上有两个羟基不稳定,脱水生成醛,则X的结构简式
,F和NaOH水溶液发生取代反应,得到的产物中一个碳原子上有两个羟基不稳定,脱水生成醛,则X的结构简式 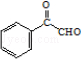 ,Y和H2发生加成反应生成M,结合环扁桃酯的结构简式,则Y的结构简式为
,Y和H2发生加成反应生成M,结合环扁桃酯的结构简式,则Y的结构简式为 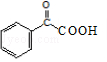 ,M的结构简式为
,M的结构简式为 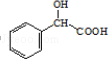 ,(1)由以上分析可知,A的结构简式是
,(1)由以上分析可知,A的结构简式是 ![]() ,所以答案是:
,所以答案是: ![]() ;(2)B的结构简式为CH3CH2OH,D的结构简式为CH3CHO,故B→D的化学方程式是2CH3CH2OH+O2
;(2)B的结构简式为CH3CH2OH,D的结构简式为CH3CHO,故B→D的化学方程式是2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O,所以答案是:2CH3CH2OH+O2
2CH3CHO+2H2O,所以答案是:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O;(3)①由以上分析可知,E的结构简式是
2CH3CHO+2H2O;(3)①由以上分析可知,E的结构简式是 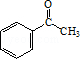 ,所以答案是:
,所以答案是:  ;②由以上分析可知,E→F的反应类型是取代反应,所以答案是:取代反应;(4)由以上分析可知,X的结构简式是
;②由以上分析可知,E→F的反应类型是取代反应,所以答案是:取代反应;(4)由以上分析可知,X的结构简式是 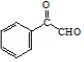 ,所以答案是:
,所以答案是:  ;(5)X的结构简式为
;(5)X的结构简式为  ,在试剂a的作用下生成Y,
,在试剂a的作用下生成Y, 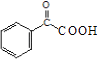 ,故X→Y发生氧化反应,则试剂a为O2 , 所以答案是:O2;(6)生成环扁桃酯的化学方程式是
,故X→Y发生氧化反应,则试剂a为O2 , 所以答案是:O2;(6)生成环扁桃酯的化学方程式是 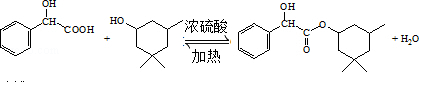 ,所以答案是:
,所以答案是:  ;(7)由CH3CH=CH2、CH3CHO为有机原料,合成CH2=CHCH=CHCH3 , 可以用CH3CH=CH2和Br2在光照的条件下发生取代反应生成BrCH2CH=CH2 , 再与镁、乙醚作用生成
;(7)由CH3CH=CH2、CH3CHO为有机原料,合成CH2=CHCH=CHCH3 , 可以用CH3CH=CH2和Br2在光照的条件下发生取代反应生成BrCH2CH=CH2 , 再与镁、乙醚作用生成 ![]() ,再与CH3CHO及H3O+ , 作用生成
,再与CH3CHO及H3O+ , 作用生成 ![]() ,最后在浓硫酸的作用下发生脱水反应得到目标产物,故故合成路线为
,最后在浓硫酸的作用下发生脱水反应得到目标产物,故故合成路线为 ![]()
![]()
![]() ,所以答案是:
,所以答案是: ![]()
![]()
![]() .
.


科目:高中化学 来源: 题型:
【题目】已知:用Pt﹣Rh合金催化氧化NH3制NO,其反应的微观模型及含氮生成物产率随反应温度的变化曲线分别如图①、图②所示:下列说法中,不正确的是( ) 
A.400℃时,生成的产物有N2、NO、H2O
B.800℃时,反应的化学方程式是:4NH3+5O2 ![]() ?4NO+6H2O
?4NO+6H2O
C.400℃﹣800℃间,Pt﹣Rh合金对N2的吸附力逐渐减弱
D.800℃以上,发生了反应:2NO(g)?O2(g)+N2(g)△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验过程如图所示,则图③试管中的现象是( ) 
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl混合溶液aL,将它均分成两份。一份滴加硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中消耗xmolH2SO4、ymolAgNO3 . 据此得知原混合溶液中的c(Na+)为( )
A.(2y-4x) /amol·L-1
B.(y-2x) /amol·L-1
C.(2y-2x) /amol·L-1
D.(y-x) /amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li﹣CuO二次电池的比能量高、工作温度宽,性能优异,广泛应用于军事和空间领域.
(1)Li﹣CuO电池中,金属锂做极.
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣.比较Li、Na、Al分别作为电极时比能量的大小: .
(3)通过如下过程制备CuO Cu ![]() CuSO4溶液
CuSO4溶液 ![]() Cu2(OH)2CO3沉淀
Cu2(OH)2CO3沉淀 ![]() CuO
CuO
①过程Ⅰ,H2O2的作用是 .
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是 .
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%.
二者比值为1:0.8时,产品中可能含有的杂质是 , 产生该杂质的原因是 .
④过程Ⅲ反应的化学方程式是 .
(4)Li﹣CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如图2.放电时,正极的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.56g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为( )
A.0.05 mol
B.1 mol
C.1.05 mol
D.0.13 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( ) 
A.原NaOH溶液的浓度为0.1mol/L
B.通入CO2的体积为448mL
C.所得溶液的溶质成分的物质的量之比为(NaOH):(Na2CO3)=1:3
D.所得溶液的溶质成分的物质的量之比为(NaHCO3):(Na2CO3)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类使用金属材料历史悠久。下列说法不正确的是
A. 电解NaCl溶液制备NaB. 电解熔融MgCl2制备Mg
C. 钢体船外镇嵌锌板可起防腐作用D. 青铜器的材质属于含锡合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】字母A﹣F代表六种不同物质,它们之间可发生如图的转化(部分反应中生成物没有全部列出).其中D是一种强酸;E是一种常见金属,有“国防金属”的美誉,可在CO2中燃烧.分析图示回答下列问题: 
(1)A可以是或;
(2)E在CO2中燃烧的化学方程式为;
(3)D与F反应的化学方程式为 , 该反应中D表现了性;
(4)50mL 14molL﹣1物质D的溶液中加入足量的铜,充分反应后共收集到气体2.24L(标准状况下),则被还原的D的物质的量为mol,参加反应的铜的质量为g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com