
(8分)目前,我国采用“接触法”制硫酸,设备如图所示:
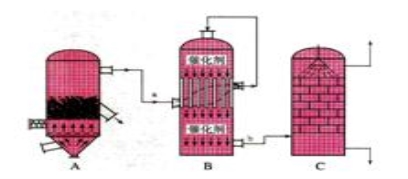
(1)图中设备A的名称是______________,该设备中主要反应的化学方程式为____________。
(2)有关接触法制硫酸的下列说法中,不正确的是______________________
A.二氧化硫的接触氧化在接触室中发生
B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫
C.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
D.硫酸工业中在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
(3)用18 mol/L 的浓硫酸配制100 mL 3.6 mol/L 稀硫酸,所需浓硫酸的体积是_______。
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源:2016届河北省高三第一次月考化学试卷(解析版) 题型:填空题
(8分)(原创)用以下几种常见有机物填写下列空白:
a.CH4
b.C2H4
c.C6H6
d.C2H5OH
e.CH3COOH
(1)等质量的CH4、C2H4、C6H6三种烃完全燃烧消耗O2的量由多到少的顺序是 (用序号表示)。
(2)等物质的量混合的甲烷和乙酸蒸气完全燃烧所得二氧化碳和水蒸气的物质的量之比为 。
(3)由乙烯和乙醇蒸气组成的混合气体1mol完全燃烧所需氧气在标准状况下的体积为 L。
(4)由两种气态烃组成的混合气体完全燃烧后,将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收)。
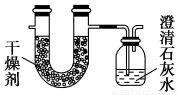
实验前 | 实验后 | |
(干燥剂+U形管)的质量 | 101.1 g | 104.7 g |
(澄清石灰水+广口瓶)的质量 | 312.0 g | 318.6 g |
根据实验数据填空:
①假设广口瓶里生成一种正盐,其质量为 g。
②混合气体中C、H两元素的物质的量之比为 。
③若混合气体是由CH4和C2H4组成,则二者的体积比为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上学期升学化学试卷(解析版) 题型:选择题
可逆反应2NO2 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ①单位时间内生成n mol O2 的同时生成2n molNO ②单位时间内生成n mol O2 的同时生成2n molNO2 ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ①单位时间内生成n mol O2 的同时生成2n molNO ②单位时间内生成n mol O2 的同时生成2n molNO2 ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
A、①④ B、②④ C、①③④ D、①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省大连市高三期初考试化学试卷(解析版) 题型:选择题
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用.下列关于硅的说法不正确的是
A.高纯度的单质硅被广泛用于制作计算机芯片
B.硅可由二氧化硅还原制得
C.常温时硅与水、空气和酸不反应,但能与氢氟酸反应
D.自然界硅元素的贮量丰富,并存在大量的单质硅
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:填空题
碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产NiOOH的一种工艺流程如下:

(1)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是 。
(2)已知Ksp[Ni(OH)2]=2×10-15,欲使NiSO4溶液中残留c(Ni2+)≤2×10-5 mol·L-1,调节pH的范围是 。
(3)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式: 。
(4)若加热不充分,制得的NiOOH中会混有Ni(OH)2,其组成可表示为xNiOOH·yNi(OH)2。现称取9.18 g样品溶于稀硫酸,加入100 mL 1.0 mol·L-1 Fe2+标准溶液,搅拌至溶液清亮,定容至200 mL。取出20.00 mL,用0.010 mol·L-1 KMnO4标准溶液滴定,用去KMnO4标准溶液20.00 mL,试通过计算确定x、y的值(写出计算过程)。涉及反应如下(均未配平):
NiOOH+Fe2++H+—Ni2++Fe3++H2O Fe2++MnO4-+H+—Fe3++Mn2++H2O
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
下图是研究铁钉腐蚀的装置图,下列说法不正确的是
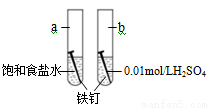
A.铁钉在两处的腐蚀速率:a < b
B.a、b两处铁钉中碳均正极
C.a、b两处铁钉中的铁均失电子被氧化
D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O
查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:填空题
硒和硫是同一主族元素,二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式: 。
(2)已知:Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O→Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是______ 。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
① SeO2+ KI+ HNO3→ Se+ I2+ KNO3+ H2O
②I2+2Na2S2O3→Na2S4O6+2NaI 配平方程式①,标出电子转移的方向和数目。
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为___ 。
查看答案和解析>>
科目:高中化学 来源:2016届江汉油田海南海政学校高三月考化学试卷(解析版) 题型:计算题
(9分)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。计算该样品中氯的物质的量,并求出FeClx中x值:________(列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品;采用上述方法测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3的物质的量分数为________。在实验中,FeCl2可用铁粉和________反应制备,FeCl3可用铁粉和________反应制备;
(3)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________;
查看答案和解析>>
科目:高中化学 来源:2016届河南省郑州市新高三年级调研检测化学试卷(解析版) 题型:选择题
已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为
A.84% B.60% C.91% D.42%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com