
| A、肥皂的主要成分是油脂 |
| B、油脂是由高级脂肪酸和甘油所生成的酯 |
| C、酶也是一种蛋白质 |
| D、蛋白质的相对分子质量通常很大,有的甚至达到几万或几百万 |
科目:高中化学 来源: 题型:

| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.20 | 20.22 | |
| 第二次 | 25.00 | 0.56 | 24.54 | |
| 第三次 | 25.00 | 0.42 | 20.40 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B、废旧电池不能随意丢弃,要进行深埋处理,防止重金属污染 |
| C、Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
| D、据测定,许多反应的温度每升高10℃,其反应速率增加2~4倍.在实验室或工业生产中,常采用加热的方法使化学反应在较高的温度下进行,以提高反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4Fe(OH)2+2H2O+O2=4Fe(OH)3↓ |
| B、2Fe+2H2O+O2=2Fe(OH)2↓ |
| C、2H2O+O2+4e-=4OH- |
| D、Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe+H2SO4=FeSO4+H2↑ |
| B、CO+CuO═Cu+CO2↑ |
| C、Cu2(OH)2CO3═2CuO+H2O+CO2↑ |
| D、4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
| a |
| 3 |
| b |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
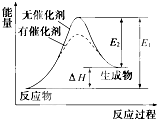 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、催化剂能改变该反应的焓变 |
| B、催化剂能降低该反应的活化能 |
| C、该反应为放热反应 |
| D、逆反应的活化能大于正反应的活化能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com