
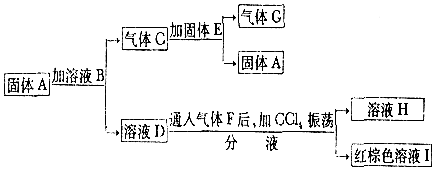
���� A��D��E��H����ɫ��Ӧ���ʻ�ɫ��������NaԪ�أ�����G��ʹ�����ǵ�ľ����ȼ����GΪO2������C�����E��Ӧ���ɹ���A����������CΪCO2��EΪNa2O2��AΪNa2CO3����ҺB�м�AgNO3��Һ����dz��ɫ����������ҺB�к�Br-����ҺH�м�AgNO3��Һ������ɫ����������ҺH�к�Cl-�����ת����ϵ��֪��BΪHBr��DΪNaBr��FΪCl2��HΪNaCl��IΪBr2���ݴ˽��
��� �⣺��1��������������֪������A����ҺB�����ʵĻ�ѧʽ�ֱ�ΪNa2CO3��HBr���ʴ�Ϊ��Na2CO3��HBr��
��2������C����E��ӦΪ2CO2+2Na2O2=2Na2CO3+O2���ʴ�Ϊ��2CO2+2Na2O2=2Na2CO3+O2��
��3������F����ҺD��Ӧ�����ӷ���ʽΪ��2Br-+Cl2=Br2+2Cl-���ʴ�Ϊ��2Br-+Cl2=Br2+2Cl-��
���� ���⿼�������ƶϣ�ע��������ʵ���ɫ�����ƶϣ���Ҫѧ����������Ԫ�ػ�����֪ʶ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Br2�ڷ�Ӧ�б��ֻ�ԭ�� | B�� | SO2�ڷ�Ӧ�б���ԭ | ||
| C�� | Br2�ڷ�Ӧ��ʧȥ���� | D�� | 1mol Br2�ڷ�Ӧ�еõ�2mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 -�������£�ij�����и����ڷ�Ӧǰ��仯��ʾ��ͼ���£����С�͡������ͬԪ�ص�ԭ�ӣ�����˵������ȷ���ǣ�������
-�������£�ij�����и����ڷ�Ӧǰ��仯��ʾ��ͼ���£����С�͡������ͬԪ�ص�ԭ�ӣ�����˵������ȷ���ǣ�������| A�� | һ������������ԭ��Ӧ | B�� | һ�����ڿ��淴Ӧ | ||
| C�� | һ�����ڷ��ȷ�Ӧ | D�� | һ���ǷֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ����������ϩ | |
| B�� | ��̼������Һ����������������� | |
| C�� | �ý�����������ˮ�Ҵ����������� | |
| D�� | ������������Һ�����Ҵ���Һ����������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ƶ�Ħ��������40 g | |
| B�� | �����Ħ����������ֵ�ϵ����������ԭ������ | |
| C�� | 1Ħ�����������ӵ�������17g/mol | |
| D�� | ������Ħ��������28 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2mol/L | B�� | 0.1mol/L | C�� | 0.6mol/L | D�� | 0.3mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ʵ���Ũ��Ϊ16.4 mol•L-1 | |
| B�� | ������50 mL��������ͭ��Ӧ�ɵõ���״����SO2 0.46 mol | |
| C�� | ijͬѧ�ø���������ϡ����ʱ��δϴ���ձ��Ͳ�������������������Ƶ�ϡ����Ũ��ƫ�� | |
| D�� | ��������ˮ���������������Һ�����ʵ���Ũ�ȴ���9.2 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | IA��Ԫ�ر�ͬ����IIA��Ԫ�صĵ�һ������С | |
| B�� | IVA��Ԫ�ص��⻯���У��ȶ�����õ���е�Ҳ��� | |
| C�� | ͬ���ڷǽ����������Ӧ��ˮ��������Դ�����������ǿ | |
| D�� | ��������Ԫ�ص����Ӱ뾶��������С |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com