
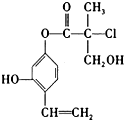
| A. | 1mol A最多可以与2mol Br2发生反应 | |
| B. | A在一定条件下可以发生消去反应和取代反应 | |
| C. | 一个A分子中最多有8个碳原子在同一平面上 | |
| D. | 1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |
分析 由结构简式可知该分子中含有酯基、醇羟基、酚羟基和碳碳双键,所以应该具有酯、醇、酚、烯烃的性质,以此解答该题.
解答 解:A.能与溴发生反应的官能团为酚羟基邻、对为氢原子的取代反应以及碳碳双键的加成,1molA最多可与3molBr2发生反应,故A错误;
B.含有-Cl,可发生消去和取代反应,另外酚羟基、酯基、羟基都可发生取代反应,故B正确;
C.苯环、碳碳双键都为平面形结构,且与苯环直接相连的原子在同一个平面上,分子中最多有10个C原子(苯环、碳碳双键、酯基)在同一个平面,故C错误;
D.能与氢氧化钠反应的官能团为酚羟基、酯基和氯原子,且酯基可水解生成酚羟基,则1molA与足量的NaOH反应,最多可以消耗4molNaOH,故D错误.
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查分析能力,明确官能团与性质的关系即可解答,熟练掌握常见有机物的官能团及其性质,难度不大.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol乙烯与乙醇的混合物在氧气中充分燃烧,消耗氧气的分子数为一定为3NA | |
| B. | 28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 0.1mol乙烷分子中含有的共价键数目为0.7NA | |
| D. | 在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①②③ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 发生硝化反应时,苯需要加热,甲苯在常温下就能进行 | |
| C. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| D. | 乙烯能发生加成反应,乙烷不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
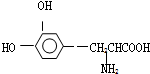 这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )| A. | 该有机物可看作氨基酸,也可看作是酚类物质 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 分子中至少有7个碳原子在同一平面内 | |
| D. | 既能与溴水发生取代反应,又能与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,其单体不可能具有的化学性质是( )
,其单体不可能具有的化学性质是( )| A. | 能使酸性KMnO4溶液褪色 | B. | 与NaOH溶液共热可生成一种钠盐 | ||
| C. | 能催化加氢生成2甲基丙酸甲酯 | D. | 能发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过品红溶液,若品红溶液褪色,则说明混有CO2气体 | |
| B. | 通过澄清石灰水,若变混浊,则说明混有CO2气体 | |
| C. | 先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体 | |
| D. | 先通过足量KMnO4溶液(具有强氧化性),再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com