
| A、分子中3个碳原子在同一直线上 | B、分子中所有原子在同一平面上 | C、与氯化氢加成只生成一种产物 | D、能使酸性KMnO4溶液褪色 |


科目:高中化学 来源: 题型:
| A、离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | B、甲醛与尿素反应得到的脲醛树脂是一种高分子黏合剂,广泛应用于木材加工业,是居室甲醛污染的主要来源 | C、目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | D、温室效应导致海水的酸度增加,珊瑚、贝壳类等生物的生存将会受到威胁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
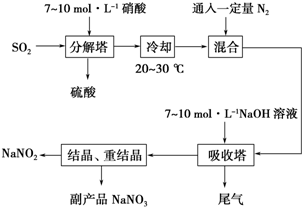
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙烯和乙烯、丁二烯互为同系物 | B、丙烯与环丙烷互为同分异构体 | C、丙烯的沸点大于乙烯 | D、理论上,等质量的聚丙烯和丙烯完全燃烧消耗的氧气相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
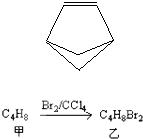 盆烯的分子结构如图所示(其中碳、氢原子均已略去).关于盆烯的说法正确的是( )
盆烯的分子结构如图所示(其中碳、氢原子均已略去).关于盆烯的说法正确的是( )| A、盆烯的一氯取代物有3种 | B、盆烯是乙烯的一种同系物 | C、盆烯是苯的一种同分异构体 | D、盆烯为不饱和烃,能与氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B40、C70都属于新型化合物 | B、C60和14C互称同位素 | C、B40、C60、C70、N60都属于烯烃 | D、B40、C60、C70、N60都只含共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:填空题
(16分)在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+ O2 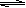 2SO3
2SO3
(1)已知:64g SO2完全转化为SO3会放出85kJ热量。SO2转化为SO3的热化学方程式是 。
(2)该反应的化学平衡常数表达式K= 。
(3)降低温度,化学反应速率 。该反应K值将 。(填“增大”或“减小”或“不变”)
(4)450℃时,在一密闭容器中,将二氧化硫与氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
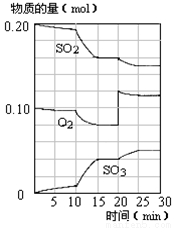
a.10-15min b.15-20min c.20-25min d.25-30min
(5)据图判断,10min到15min的曲线变化的原因可能是 (填写编号)。
a.增加SO3的物质的量 b.增大容器体积 c.降低温度 d.催化剂
(6)在15分钟时,SO2的转化率是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com