
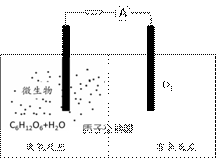
 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2=6CO2+6H2O
【答案】A
【解析】首先根据原电池反应判断出厌氧反应为负极侧,有氧反应为正极侧。A、根据厌氧反应中碳元素的化合价的变化:葡萄糖分子中碳元素平均为0价,二氧化碳中碳元素的化合价为+4价,所以生成二氧化碳的反应为氧化反应,所以在负极生成。错误;B、在微生物的作用下,该装置为原电池装置。原电池能加快氧化还原反应速率,故可以说微生物促进了电子的转移。正确;C、原电池中阳离子向正极移动。正确;D、电池的总反应实质是葡萄糖的氧化反应。正确。
【考点定位】原电池原理;难度为一般等级
【名师点晴】本题是关于能量转化的题目,电化学包括原电池和电解池。原电池是将化学能转化为电能的装置,组成有正负极、电解质溶液、形成闭合回路,活动性强的电极为负极,发生氧化反应,活动性弱的电极为正极,正极上发生还原反应。电解池是将电能转化为化学能的装置。与外加电源正极连接的为阳极,与电源负极连接的为阴极。阳极发生氧化反应,阴极发生还原反应。若阳极是活性电极,则是电极本身失去电子,若电极是惰性电极,则电解质溶液(或熔融状态)阴离子发生还原反应。掌握好阴离子、阳离子的放电顺序、清楚在闭合回路中电子转移数目相等是本题的关键。


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
已知甲醛分子中4个原子是共平面的。下列分子中所有原子不可能同时存在于同一平面上的是( )
A、CH2=CH —CH=CH2 B、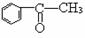
C、ClCH=CHCHO D、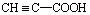
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.用钠可以检验乙醇中是否含有水
B.1 mol二甘醇(HO—CH2CH2OCH2CH2—OH)和足量的钠反应可以产生0.5 mol H2
C.乙醇和乙酸在浓硫酸加热条件下的反应是取代反应
D.葡萄糖和新制Cu(OH)2悬浊液加热沸腾生成砖红色沉淀的反应是加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关仪器使用方法或实验操作说法正确的是( )
A.滴定管和容量瓶在使用前均需检查是否漏水
B.用蒸馏水湿润的pH试纸测定溶液的pH
C.托盘天平称量药品时,都应垫上滤纸称量
D.石蕊、酚酞均可用作中和滴定的指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
Fridel-Crafts反应是向苯环上引入烷基最重要的方法,在合成上有很大的实用价值,该反应可以简单表示如下:ArH+RX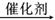 ArR+HX;△H<0(Ar表示苯基)。某化学兴趣小组在实验室先利用叔丁醇与盐酸反应制得叔丁基氯(沸点50.7℃),再利用Fridel-Crafts反应原理制备对叔丁基苯酚(熔点99℃)。反应流程及实验装置如下图所示:
ArR+HX;△H<0(Ar表示苯基)。某化学兴趣小组在实验室先利用叔丁醇与盐酸反应制得叔丁基氯(沸点50.7℃),再利用Fridel-Crafts反应原理制备对叔丁基苯酚(熔点99℃)。反应流程及实验装置如下图所示:
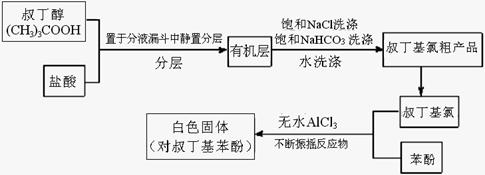
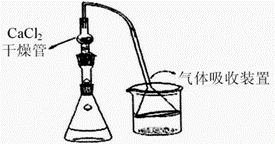
试回答下列问题:
(1)步骤①是直接将盐酸、叔丁醇直于分液漏斗中,振摇一段时间后静置分液。振摇过程中应进行_____________操作。步骤②中用饱和食盐水及饱和碳酸氢钠的目的是__________________。步骤③是要将叔丁基氯粗产品制成精品,实验操作方法是________________________。
(2)步骤④在如图装直中进行,若实验过程中去掉制备装置中装有氯化钙的干燥管,有可能导致的不良后果是________________________。
(3)叔丁基氯与苯盼反应时适当控制温度是很重要的。若反应过程中温度过高应用冷水浴冷却,否则可能导致的不良后果是__________________________。
(4)常温下叔丁基氯易变质(打开瓶塞时瓶口会有白雾现象〉,故实验中所用的必须现用现配,试写出叔丁基氯在常温下变质时发生反应的化学方程式______________________。
 (5)实验中得到产品叔丁基苯盼常常不是白色而呈现浅紫色,你认为可能的原因是_______________。
(5)实验中得到产品叔丁基苯盼常常不是白色而呈现浅紫色,你认为可能的原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某模拟"人工树叶”电化学实验装置如右图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
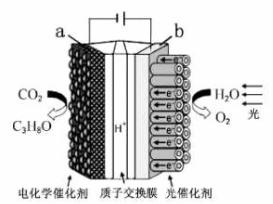
A.该装置将化学能转化为光能和电能
B.该装置工作时,H+从b极区向a极区迁移
C.每生成1 mol O2,有44 g CO2被还原
D.a电极的反应为:3CO2 + 16H+-18e-= C3H8O+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al_____Si | N____O | 金刚石_____晶体硅 | CH4____SiH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为------------------------------------------------------------------------ ----------------------------( )
----------------------------( )
 A 2 mol Br2 2 mol NaOH B 2 mol Br2 3 mol NaOH
A 2 mol Br2 2 mol NaOH B 2 mol Br2 3 mol NaOH
C  3 mol Br2 4 mol NaOH D 4 mol Br2 4 mol NaOH
3 mol Br2 4 mol NaOH D 4 mol Br2 4 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
经测定由C3H7OH和C6H12组成的混合物中氧的质量分数为8%,则此混合物中氢的质量分数是------------------------------------------------------------------------------------------------------( )
A.78% B.22% C.14% D.13%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com