
| A���ѺϽ���һ�����ͽ������� |
| B���ѺϽ��۵�ȳɷֽ����ߣ���Ӳ��Ҳ���� |
| C��Ŀǰ����ʹ����㷺�Ľ������������Ͻ� |
| D����ͭ��̼�ظ֡��Ͻ�ֺ�Ӳ�����ǺϽ� |


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��v��B2��=0.8mol?L-1?S-1 |
| B��v��B2��=0.42mol?L-1?S-1 |
| C��v��C��=0.6mol?L-1?S-1 |
| D��v��A2��=0.4mol?L-1?S-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2NO2��g��?N2O4��g����H��0 |
| B��3O2��g��?2O3��g����H��0 |
| C��H2��g��+I2��g��?2HI��g����H��0 |
| D��NH4HCO3��s��?NH3��g��+H2O��g��+CO2��g����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
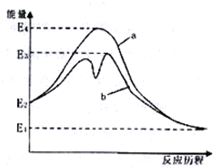 ��ͼ��ʾ������ij��Ӧ��ܵ�Ӱ�죮������ĵ��볣�����£�HClO Kw=2.95��10-8��
��ͼ��ʾ������ij��Ӧ��ܵ�Ӱ�죮������ĵ��볣�����£�HClO Kw=2.95��10-8��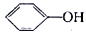 Kw=1.02��10-10H2CO3 Ka1=4.30��10-7 Ka2=5.61��10-11����ͼ��������жϣ�����˵��������ǣ�������
Kw=1.02��10-10H2CO3 Ka1=4.30��10-7 Ka2=5.61��10-11����ͼ��������жϣ�����˵��������ǣ�������| A��ͼ˵���˴������뻯ѧ��Ӧ���������˻�� |
| B��ͼ�и÷�Ӧû�д�������ʱ���ΪE2-E1 |
| C��������CO2ͨ��NaClO��Һ�У��������·�ӦNaClO+CO2+H2O�THClO+NaHCO 3 |
D����ͬŨ�ȵ�NaClO��Һ��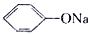 ��Һ��ǰ��pHС ��Һ��ǰ��pHС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Դ���п�����������Ⱦ���ص㣬����Ӧ�����ᳫ����̫���ܡ����ܺ��������� |
| B���Ӹ߹������̴ѣ�ʹ�̳��ͷ���Զ��ر����ɼ��ٻ�����Ⱦ |
| C�������÷ֹ��ȼƣ�ͨ����ɫ���ⶨ��ѧ��Ӧ���� |
| D���ں����������п�飬�ɼ�������ĸ�ʴ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ƭ��ϡ����ķ�Ӧ |
| B��Ba��OH��2��8H2O��NH4Cl�ķ�Ӧ |
| C�����ȵ�̿��CO2�ķ�Ӧ |
| D�������������е�ȼ�շ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| �� |
| ��ѧ�� | H-Cl | O=O | Cl=Cl | H-O |
| ����/kJ��mol-1 | 431 | 498 | 243 | 463 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ԫ�ص�ԭ������������Խ�٣����Ԫ�صĽ�����Խǿ |
| B��ͬ����Ԫ��ԭ�Ӱ뾶�����Ӱ뾶�����Ҿ����μ�С |
| C���������ڷǽ����������Ӧˮ��������Դ�����������ǿ |
| D���ڢ�A��Ԫ����̬�⻯��Ļ�ԭ�Դ��ϵ���������ǿ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com