
| A. | I2、Br2、Cl2 | B. | Na+、K+、Cs+ | C. | Cl-、Br-、I- | D. | Al3+、Mg2+、Na+ |
分析 金属元素的金属性越强,则单质的还原性越强,非金属元素的非金属性越强,则其原子和阴离子的还原性越弱,金属离子处于最高价时只有氧化性,没有还原性.
解答 解:A、非金属元素的非金属性越强,则其原子的还原性越弱,F、Cl、Br的非金属性逐渐减弱,则Cl2、Br2、I2的还原性增强,故A错误;
B、金属元素的金属性越强,则单质的还原性越强,Na、K、Cs的金属性逐渐增强,则Na+、K+、Cs+的氧化性逐渐减弱,故B错误;
C、非金属元素的非金属性越强,则其阴离子的还原性越弱,Cl、Br、I的非金属性逐渐减弱,则Cl-、Br-、I-的还原性增强,故C正确;
D、金属离子处于最高价时只有氧化性,没有还原性,则不能比较Mg2+、Al3+、Na+的还原性,故D错误.
故选C.
点评 本题考查还原性强弱比较,明确金属性、非金属性与还原性的关系即可解答,题目难度不大,注意把握同主族、同周期元素性质的递变规律.


科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA | |
| B. | 2.24 L二氧化碳中含有共价键数目为4NA | |
| C. | 7.1g Cl2与足量NaOH 溶液反应转移的电子数为0.2NA | |
| D. | 1 mol NH4+中含有电子数为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 起始浓度/mol•L-1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | X | 0.2 | 7 |
| A. | 实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+) | |
| B. | 实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=$\frac{{K}_{W}}{1×1{0}^{-5}}$mol•L-1 | |
| C. | 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol•L-1 | |
| D. | 实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
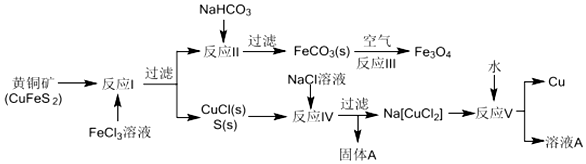
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
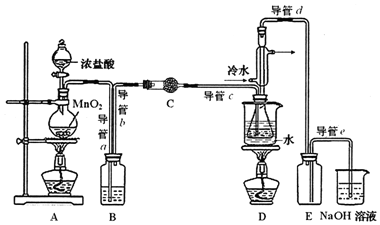
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| S | 113 | 444 | 1.96 | 不溶于水 |
| S2Cl2 | -76 | 138 | 1.75 | 与水反应 |
| CS2 | -109 | 47 | 1.26 | 不溶于水 |
| CCl4 | -23 | 77 | 1.59 | 不溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑦ | B. | ②③⑤⑦ | C. | ①④⑥⑦ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
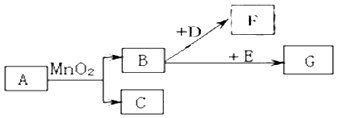
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com