
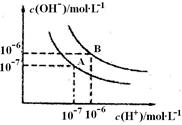
科目:高中化学 来源:不详 题型:单选题
| A.多余的氧气中 |
| B.生成的三氧化硫中 |
| C.氧气和二氧化硫中 |
| D.二氧化硫、氧气和三氧化硫中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 1 |
| 2 |
| 1 |
| 2 |
| A.吸热88kJ | B.吸热44kJ |
| C.放热44kJ | D.吸热2.44kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度  I— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3—的总浓度,设为c1,c1 = c(I2)+c(I3—);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)= c2,c(I3—)=c1 —c2;
I— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3—的总浓度,设为c1,c1 = c(I2)+c(I3—);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)= c2,c(I3—)=c1 —c2;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=4的醋酸中:c(H+)=4.0molL-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中, |
D.混合溶液中, |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=4的醋酸中:c(H+)=4.0mol·L-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 序号 | 氢氧化钡的体积/mL | 硫酸氢钠的体积/mL | 溶液的pH |
| ① | 33.00 | 0.00 | 8 |
| ② | 33.00 | x | 7 |
| ③ | 33.00 | 33.00 | 6 |
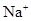 )>c(
)>c(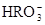 )>c(
)>c(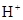 )>c(
)>c(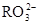 )>c(
)>c(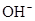 )
)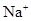 )+c(
)+c(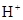 )=c(
)=c(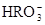 )+2c(
)+2c(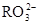 )+c(
)+c(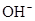 )
)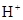 )+c(
)+c(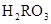 )=c(
)=c(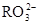 )+c(
)+c(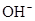 )
)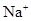 )、c(
)、c(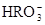 )、c(
)、c(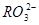 )分别相等
)分别相等查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合前CH3COONa溶液中由水电离出来的c(OH—)>1×10-7 mol·L-1 |
| B.混合前NaCl溶液中:c(Na+) + c(OH—)= c(Cl-)+c(H+) |
| C.混合溶液中 :c(Cl-) >c(CH3COOH) >c(OH—) |
| D.混合溶液中:c(Cl-) + c(CH3COO-) =0.1mol·L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com