
| A、C | B、Al | C、O | D、Si |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、为了防止蛋白质盐析,疫苗等生物制剂应冷冻保存 |
| B、玻璃、陶瓷、水泥都是硅酸盐产品,属于无机非金属材料 |
| C、玉兔号月球车电池帆板,可以将化学能转换成电能 |
| D、弱酸性或中性条件下,钢铁腐蚀的正极反应式为:4OH--4e-=O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2的消耗速率与NO的生成速率相等 |
| B、容器内NO2的物质的量与NO的物质的量相等 |
| C、NO2和O2的消耗速率之比为2:1 |
| D、单位时间内生成2n molNO.同时生成n molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有SO32-离子 |
| B、一定有Cl-离子 |
| C、一定有CO32-离子 |
| D、不能确定HCO3-离子是否存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
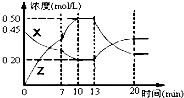 向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g)△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g)△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )| A、用X表示0~10min内该反应的平均速率为v(X)=0.045mol/(L?min) |
| B、化学方程式中a:b=1:3 |
| C、推测在第7min时曲线变化的原因可能是增加X的浓度 |
| D、推测该反应处于化学平衡状态的时间是10min--13min及第20min后 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用.
高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用.| a | b | c | |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com