
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
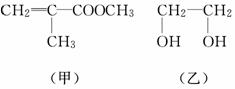
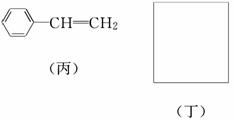
填写下列空白:
(1)甲中不含氧原子的官能团是________;下列试剂能与甲反应而褪色的是________(填标号)。
a.Br2/CCl4溶液 b.石蕊溶液
c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:________。
(3)淀粉通过下列转化可以得到乙(其中A~D均为有机物):
淀粉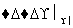 A
A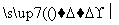 B
B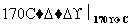 C
C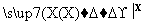 D
D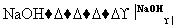 乙
乙
A的分子式是________,试剂X可以是________。
(4)已知:
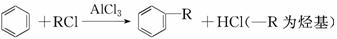
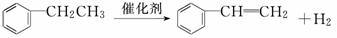
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是__________________________________________________________
________________________________________________________________________。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为________。
解析:本题考查了有机物的结构、性质等方面的知识,同时考查了考生的分析推理能力。
(1)甲物质中的碳碳双键能与单质溴加成,能被酸性KMnO4溶液氧化,a、c符合条件。
(3)淀粉水解生成葡萄糖,A的分子式为C6H12O6,B为乙醇,C为乙烯,乙烯与卤素单质加成生成二卤代物D,D水解得到乙二醇,故试剂X是卤素单质。
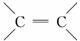 (4)合成过程为乙烯先与HCl加成生成氯乙烷,然后氯乙烷与苯发生取代反应生成乙苯,乙苯再发生消去反应得到丙。
(4)合成过程为乙烯先与HCl加成生成氯乙烷,然后氯乙烷与苯发生取代反应生成乙苯,乙苯再发生消去反应得到丙。
答案:(1)碳碳双键(或 ) a、c
(2)CH2===CHCH2CH2COOH(或其他合理答案)
(3)C6H12O6 Br2/CCl4(或其他合理答案)


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
工业上为了处理含有Cr2O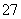 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准。关于上述方法,下列说法错误的是( )
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准。关于上述方法,下列说法错误的是( )
A.阳极反应:Fe-2e-===Fe2+
B.阴极反应:2H++2e-===H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
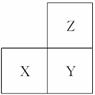 短周期元素X、Y、Z在周期表中的位置如图所示。下列说法正确的是( )
短周期元素X、Y、Z在周期表中的位置如图所示。下列说法正确的是( )
A.若它们均为金属元素,则X与氧元素组成的物质中一定只含离子键
B.若它们的原子最外层电子数之和为11,则它们均为非金属元素
C.它们的原子最外层电子数的大小顺序一定是Z=Y>X
D.Z元素的最高化合价不一定大于X元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一些常见有机物的转化关系,关于反应①~⑦的说法不正确的是( )

A.反应①是加成反应
B.只有反应②是加聚反应
C.只有反应⑦是取代反应
D.反应④⑤⑥是取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
现有六种有机物:①乙醇、②苯酚、③溴乙烷、④乙烯、⑤乙酸、⑥甲酸乙酯,其中(填写序号):
(1)一定条件下能发生银镜反应的是________。
(2)一定条件下能发生消去反应的是________。
(3)一定条件下能与H2发生加成反应的是________。
(4)一定条件下能与NaOH溶液发生反应的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物( )
A.所含公用电子对数目为(a/7+1)NA
B.所含碳氢键数目为aNA/7
C.燃烧时消耗的O2一定是33.6 a/14 L
D.所含原子总数为aNA/14
查看答案和解析>>
科目:高中化学 来源: 题型:
有关下 图所示化合物的说法不正确的是( )
图所示化合物的说法不正确的是( )
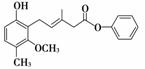
A.该化合物既可以催化加氢,又可以在光照下与Cl2发生取代反应
B.该化合物既可以与溴水反应,又可以使酸性KMnO4溶液褪色
C.该化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
D.1 mol该化合物最多可以与2 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.CH3COOH与CH3COONa混合溶液中,一定有c(CH3COO-) >c(Na+)
B.向新制氯水中加入CaCO3可使溶液中HClO浓度增大
C.AgCl在200ml 0.1mol/LNaCl中的溶解度小于在50ml 0.1mol/LMgCl2中溶解度
D.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气中,产生NO的反应为:N2(g)+O2(g) 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
A.温度T下,该反应的平衡常数K=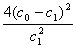
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com