
金属元素及其化合物在科学研究和生产生活中有着广泛的用途。
(1)现有一种铜粉与氧化铜粉末的混合物。经测定,该混合物中铜元素与氧元素的质量之比为5:1。该混合物中铜与氧化铜的物质的量之比为 。
(2)取铝合金(含铝90%)1.5 g 与80 mL 3mol•L-1 盐酸充分反应(合金中其它成分不参加反应)。滤去不溶物,将滤液稀释到100mL,取出稀释液5mL,加入0.6 mol•L-1 的氨水使Al3+ 恰好完全沉淀。
上述铝合金和盐酸反应的过程中生成氢气_________L(标准状况)。使Al3+ 恰好完全沉淀时,消耗氨水_________mL。
(3)将1.84g金属钠投入98.16 g水中,向反应后的溶液里通入一定量的CO2(g),将溶液小心蒸干。计算可得固体质量的最大值。
(4)向a mL 0.8mol•L-1 NaOH(aq) 中通入b mol CO2(g),反应所得混合液的成份随b的物质的量的不同而不同。请通过计算完成下表:(溶质的质量用含a、b的代数式表示)
|
b的取值范围(mol) |
溶质的成份 |
溶质的质量(g) |
|
b<4a×10- 4 |
|
|
|
|
Na2CO3、NaHCO3 |
|
(1)1:4 (2分)
(2)1.68L (2分) 20mL (2分)
(3)11.44g(2分,过程1分,结果1分)
(4)
|
b的取值范围(mol) |
溶质的成份 |
溶质的质量(g) |
|
|
NaOH、Na2CO3 (1分,每个0.5分) |
3.2a×10-2+26b(2分) |
|
8a×10-4>b>4a×10-4(1分) |
|
1.76a×10-2+62b(2分) |
【解析】
试题分析:(1)设铜粉与氧化铜粉末的物质的量分别为X,Y。根据该混合物中铜元素与氧元素的质量之比为5:1。建立关系式64(X+Y):16Y=5:1,可得X:Y=1:4。
(2)铝的物质的量为1.5*90%/27=0.05mol,n(HCl)=0.08*3=0.24mol,可知盐酸剩余,生成氢气0.05mol*1.5*22.4=1.68L。使Al3+ 恰好完全沉淀时,首先要中和剩余的盐酸0.09mol,消耗氨水(0.05*3+0.09)/(0.6*20)=20mL。
(3)将1.84g金属钠(0.08mol)投入98.16 g水中,向反应后的溶液里通入一定量的CO2(g),将溶液小心蒸干。计算可得固体质量的最大值。要使固体的质量最大,生成物应该是Na2CO3.10H2O ,根据钠元素守恒,生成物质的量为0.04mol,质量为0.04*286=11.44g。
(4)NaOH物质的量为8a×10-4mol,由 CO2和NaOH反应的关系式,n(NaOH):n(CO2)>=2,产物为碳酸钠和剩余的氢氧化钠,即8a×10-4mol:b>=2,可得b<=4a×10-4。根据2NaOH-----nCO2关系,生成碳酸钠和剩余的氢氧化钠分别为bmol和8a×10-4mol-2bmol,其质量为:3.2a×10-2+26b;当1<n(NaOH):n(CO2)<2时,产物是Na2CO3和NaHCO3根据钠和碳元素守恒,分别设Na2CO3和NaHCO3的物质的量为x,y,可建立关系式:2x+y=8a×10-4mol; x+y=b;求得混合物质量为1.76a×10-2+62b。
考点:本题考查了根据化学方程式进行计算,涉及到元素守恒法在解题的中运用。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 | A | 铁是地壳中含量最高的 金属元素 |
铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 | B | 常温下铁与稀硫酸反应 生成氢气 |
高温下氢气能还原氧化 铁得到铁 |
Ⅰ对;Ⅱ对;无 | C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 | D | 在空气中铁的表面能形 成致密的氧化膜 |
铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 过渡金属元素及其化合物的应用研究是目前科学研究的前沿之一.试回答下列问题:
过渡金属元素及其化合物的应用研究是目前科学研究的前沿之一.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
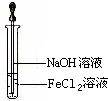 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:
 铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料.
铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料.

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com