
| A. | 乙烷和氯气发生二氯取代反应,所得产物只有一种 | |
| B. | 糖类水解的最终产物一定是葡萄糖 | |
| C. | 淀粉和纤维素的组成都可以用(C6H10O5)n表示,所以它们既是同系物又是同分异构体 | |
| D. | 油脂是食物组成中的重要部分,也是产生能量最高的营养物质 |
分析 A、乙烷和氯气发生二氯取代的产物有两种;
B、蔗糖水解为葡萄糖和果糖;
C、淀粉和纤维素的下标n的取值范围不同;
D、油脂是营养物质之一,是供能最高的物质.
解答 解:A、乙烷和氯气发生二氯取代的产物有两种,即1,1-二氯乙烷和1,2-二氯乙烷,故A错误;
B、蔗糖水解为葡萄糖和果糖,即糖类水解的最终产物不一定是葡萄糖,故B错误;
C、淀粉和纤维素的下标n的取值范围不同,故淀粉和纤维素的分子式不同,不是同分异构体,也不是同系物,故C错误;
D、油脂是六大营养物质之一,是供能最高的物质,是人体必需的营养物质,故D正确.
故选D.
点评 本题考查了糖类、油脂和烃的有关性质,应注意的是糖类不一定均能水解,水解的最终产物也不一定均为葡萄糖.


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
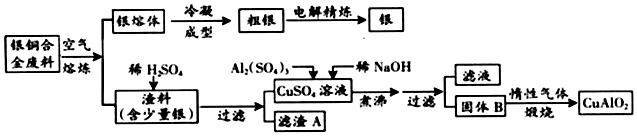
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三氧化二铁中有少量的氧化铝:加过量的烧碱溶液后过滤洗涤 | |
| B. | 氯化钠中有少量的I2:通过加热的方法 | |
| C. | CO中有少量的CO2:用氢氧化钠洗涤后再干燥 | |
| D. | 食盐中有少量的氧化铝:加过量的烧碱溶液后蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①Ⅰ | B. | ②Ⅱ | C. | ③Ⅲ | D. | ④Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
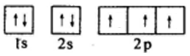 ,D的电子排布式为1s22s22p63s23p2.
,D的电子排布式为1s22s22p63s23p2.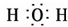 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


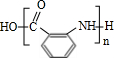 .
. .
. 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 最合理的方案.
最合理的方案.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入几滴硫酸铜溶液 | B. | 加入适量的水 | ||
| C. | 加入适量NaCl溶液 | D. | 再加入少量稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com