
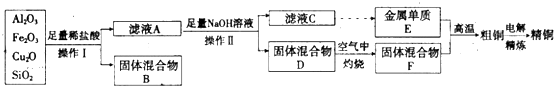
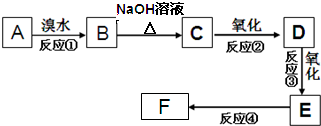
·ÖĪö æóŌüŗĶŃĪĖį·“Ó¦£¬Ńõ»ÆĀĮ”¢Ńõ»ÆŃĒĶŗĶŃõ»ÆĢśÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆĪļ£¬Ńõ»ÆŃĒĶŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆĶŗĶĶ£¬¶žŃõ»Æ¹čŗĶŃĪĖį²»·“Ó¦£¬ĖłŅŌ¹ĢĢå»ģŗĻĪļBÓŠĶŗĶ¶žŃõ»Æ¹č£¬ĀĖŅŗAŗ¬ÓŠĀČ»ÆŃĒĢś”¢ĀČ»ÆĶŗĶĀČ»ÆĀĮ£»ĻņĀĖŅŗAÖŠ³äČė¹żĮæĒāŃõ»ÆÄĘ£¬Éś³ÉĒāŃõ»ÆĢś”¢ĒāŃõ»ÆĶ³Įµķ£¬Ķ¬Ź±Éś³ÉĘ«ĀĮĖįÄĘ£¬ĖłŅŌ¹ĢĢå»ģŗĻĪļDŹĒĒāŃõ»ÆĢśŗĶĒāŃõ»ÆĶ£¬ĀĖŅŗCŹĒĘ«ĀĮĖįÄĘŗĶĒāŃõ»ÆÄĘČÜŅŗ£»ĒāŃõ»ÆĢśŗĶĒāŃõ»ÆĶŌŚæÕĘųÖŠ×ĘÉÕÉś³ÉŃõ»ÆĶŗĶŃõ»ÆĢś£¬ĖłŅŌ¹ĢĢå»ģŗĻĪļFŹĒŃõ»ÆĶŗĶŃõ»Æ Ģś£»Ę«ĀĮĖįÄĘČÜŅŗµĆµ½µÄµ„ÖŹEŹĒ½šŹōĀĮ£¬
£Ø1£©øł¾Ż·ÖĄėČÜŅŗŗĶ³Įµķ£»øł¾Ż×ĘÉÕ¹ż³ĢĖłŠčŅŖÓƵ½µÄŅĒĘ÷·ÖĪö¼“æÉ£»
£Ø2£©ŅĄ¾ŻĢįČ”Į÷³ĢĶ¼æÉÖŖ£¬¼ÓČė¹żĮæŃĪĖį£¬Ńõ»ÆĢśŗĶŃõ»ÆĀĮČ«²æČܽāĪŖĀČ»ÆĢśŗĶĀČ»ÆĀĮČÜŅŗ£¬Cu2OÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆĶ”¢ĶŗĶĖ®£¬Éś³ÉµÄĶÄÜÓėĀČ»ÆĢś·“Ӧɜ³ÉĀČ»ÆŃĒĢśŗĶĀČ»ÆĶ£¬¶žŃõ»Æ¹č²»ČÜÓŚŃĪĖįĪŖ³Įµķ£»Čż¼ŪĢśĄė×ÓÓėKSCNČÜŅŗ·¢Éś·“Ӧɜ³ÉŗģÉ«ĪļÖŹĄ“¼ģŃéČż¼ŪĢśĄė×Ó£»
£Ø3£©øł¾ŻĀĮČČ·“Ó¦µÄŌĄķĄ“ŹéŠ“£»
£Ø4£©ÉčČÜŅŗµÄPHĪŖX£¬Č»ŗóĒó³öÓÉĖ®µēĄė³öµÄc£ØOH-£©£¬ĄūÓĆÓÉĖ®µēĄė³öµÄc£ØOH-£©Ē°ÕßĪŖŗóÕßµÄ108±¶Ēó³öX£»
£Ø5£©¢Ła£®µēÄÜ×Ŗ»ÆĪŖ»ÆѧÄÜ”¢ČČÄÜ£»
b£®“ÖĶ½ÓµēŌ“Õż¼«£¬Ź§Č„µē×Ó£¬·¢ÉśŃõ»Æ·“Ó¦
c£®¾«Ķ×÷Ņõ¼«£¬µē½āŗóµē½āŅŗÖŠCu2+ÅØ¶Č¼õŠ”
d£®“ÖĶ¾«Į¶Ź±ĶعżµÄµēĮæÓėŅõ¼«Īö³öĶµÄĮæ“ęŌŚ¹ŲĻµ£»
¢ŚŅŖ²ā¶ØĶµÄÖŹĮæ·ÖŹż£¬æÉŅŌ°ŃÅØĮņĖįĻ”ŹĶ£¬ĶŗĶĻ”ĮņĖį²»·“Ó¦£¬Ńõ»ÆĶŗĶĻ”ĮņĖį·“Ó¦£¬¼“æÉĒó³öĶµÄÖŹĮæ·ÖŹż£®Éč¼Ę·½°øµÄÖ÷ŅŖ²½ÖčŹĒ½«ÅØĮņĖįÓĆÕōĮóĖ®Ļ”ŹĶ£¬½«ŃłĘ·ÓėĻ”ĮņĖį³ä·Ö·“Ó¦ŗ󣬹żĀĖ£¬øÉŌļ£¬³ĘĮæŹ£Óą¹ĢĢåĶµÄÖŹĮ漓æÉ£»
½ā“š ½ā£ŗ£Ø1£©ŹµŃé²Ł×÷I²½ÖčÖŠ·ÖĄėČÜŅŗŗĶ³ĮµķµÄ²Ł×÷Ćū³ĘĪŖ¹żĀĖ£¬ŌŚæÕĘųÖŠ×ĘÉÕ¹ĢĢå»ģŗĻĪļDŹ±£¬ĖłÓƵ½µÄŅĒĘ÷ÓŠŪįŪö”¢ÄąČż½Ē”¢Čż½Ē¼Ü”¢¾Ę¾«µĘ£¬²£Į§°ō£¬
¹Ź“š°øĪŖ£ŗ¹żĀĖ£»ŪįŪö£»
£Ø2£©ŅĄ¾ŻĢįČ”Į÷³ĢĶ¼æÉÖŖ£¬¼ÓČė¹żĮæŃĪĖį£¬Ńõ»ÆĢśŗĶŃõ»ÆĀĮČ«²æČܽāĪŖĀČ»ÆĢśŗĶĀČ»ÆĀĮČÜŅŗ£¬Cu2OÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆĶ”¢ĶŗĶĖ®£¬Éś³ÉµÄĶÄÜÓėĀČ»ÆĢś·“Ӧɜ³ÉĀČ»ÆŃĒĢśŗĶĀČ»ÆĶ£¬·½³ĢŹ½ĪŖ£ŗ2FeCl3+CuØT2FeCl2+CuCl2£¬¶žŃõ»Æ¹č²»ČÜÓŚŃĪĖįĪŖ³Įµķ£¬ĖłŅŌĀĖŅŗAÖŠĢśŌŖĖŲµÄ“ęŌŚŠĪŹ½ĪŖŃĒĢśĄė×Ó£¬æÉÓĆĀČĖ®½«ĘäŃõ»Æ³ÉČż¼ŪĢśĄė×Ó£¬Čż¼ŪĢśĄė×ÓÓėKSCNČÜŅŗ·¢Éś·“Ӧɜ³ÉŗģÉ«ĪļÖŹĄ“¼ģŃéČż¼ŪĢśĄė×Ó£¬
¹Ź“š°øĪŖ£ŗFe2+£»2Fe3++CuØT2Fe2++Cu2+£»KSCNČÜŅŗ”¢ĀČĖ®£»
£Ø3£©ĀĮÓėŃõ»ÆĢś·¢ÉśĀĮČČ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Al+Fe2O3$\frac{\underline{\;øßĪĀ\;}}{\;}$Al2O3+2Fe£¬
¹Ź“š°øĪŖ£ŗ2Al+Fe2O3$\frac{\underline{\;øßĪĀ\;}}{\;}$Al2O3+2Fe£»
£Ø4£©ÉčČÜŅŗµÄPHĪŖX£¬NaAlO2ČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØOH-£©=10X-14mol/L£¬NaOHČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØOH-£©=10-Xmol/L£¬$\frac{10{\;}^{X-14}}{10{\;}^{-X}}$=108£¬½āµĆX=11£¬
¹Ź“š°øĪŖ£ŗ11£»
£Ø5£©£©¢Ła£®µēÄܲæ·Ö×Ŗ»ÆĪŖ»ÆѧÄÜ£¬¹Źa“ķĪó£»
b£®“ÖĶ½ÓµēŌ“Õż¼«£¬Ź§Č„µē×Ó£¬·¢ÉśŃõ»Æ·“Ó¦£¬¹ŹbÕżČ·£»
c£®¾«Ķ×÷Ņõ¼«£¬µē½āŗóµē½āŅŗÖŠCu2+ÅØ¶Č¼õŠ”£¬¹ŹcÕżČ·£»
d£®“ÖĶ¾«Į¶Ź±ĶعżµÄµēĮæÓėŅõ¼«Īö³öĶµÄĮæ“ęŌŚ¹ŲĻµ£ŗµēĀ·ÖŠĶعż3.01”Į1023øöµē×Ó£¬µĆµ½¾«ĶµÄÖŹĮæĪŖ16g£¬¹Źd“ķĪó£»
¹ŹŃ”£ŗb”¢c£»
¢ŚŅŖ²ā¶ØĶµÄÖŹĮæ·ÖŹż£¬æÉŅŌ°ŃÅØĮņĖįĻ”ŹĶ£¬ĶŗĶĻ”ĮņĖį²»·“Ó¦£¬Ńõ»ÆĶŗĶĻ”ĮņĖį·“Ó¦£¬¼“æÉĒó³öĶµÄÖŹĮæ·ÖŹż£®Éč¼Ę·½°øµÄÖ÷ŅŖ²½ÖčŹĒ½«ÅØĮņĖįÓĆÕōĮóĖ®Ļ”ŹĶ£¬½«ŃłĘ·ÓėĻ”ĮņĖį³ä·Ö·“Ó¦ŗ󣬹żĀĖ£¬øÉŌļ£¬³ĘĮæŹ£Óą¹ĢĢåĶµÄÖŹĮ漓æÉ£»
¹Ź“š°øĪŖ£ŗ½«ÅØĮņĖįÓĆÕōĮóĖ®Ļ”ŹĶ£¬½«ŃłĘ·ÓėĻ”ĮņĖį³ä·Ö·“Ó¦ŗó£®
µćĘĄ ±¾ĢāŅŌæóŌü£Øŗ¬ÓŠCu2O”¢Al2O3”¢Fe2O3”¢SiO2£©ĢįČ”ĶĪŖ±³¾°£¬Ö÷ŅŖæ¼²éĮĖĪļÖŹµÄŠŌÖŹ”¢»Æѧ·½³ĢŹ½”¢µē½āŌĄķµČ£¬ÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 25”ꏱ£¬ŅŃÖŖH2CO3?H++HCO3-K1=4.3”Įl0-7£»
25”ꏱ£¬ŅŃÖŖH2CO3?H++HCO3-K1=4.3”Įl0-7£»| A£® | WµćĖłŹ¾µÄČÜŅŗÖŠ£ŗc£ØNa+£©+c£ØH+£©=2c£ØCO32-£©+c£ØOH-£©+c£ØHCO3-£© | |
| B£® | pH=4µÄČÜŅŗÖŠ£ŗc£ØH2CO3£©+c£ØHCO3-£©+c£ØCO32-£©=0.1 mol•L-1 | |
| C£® | pH=8µÄČÜŅŗÖŠ£ŗc£ØH+£©+c£ØH2CO3£©+c£ØHCO3-£©=c£ØOH-£©+c£ØCl-£© | |
| D£® | pH=11µÄČÜŅŗÖŠ£ŗCO32-+H2O?HCO3-+OH-K=1.8”Įl0-4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĢģČ»Čõ¼īŠŌĖ®³Ź¼īŠŌµÄŌŅņŹĒĘäÖŠŗ¬ÓŠ½Ļ¶ąµÄMg2+”¢Ca2+µČĄė×Ó | |
| B£® | µ°°×ÖŹ”¢µķ·ŪŗĶÓĶÖ¬¶¼ŹōÓŚøß·Ö×Ó»ÆŗĻĪļ£¬Ņ»¶ØĢõ¼žĻĀ¶¼ÄÜĖ®½ā | |
| C£® | ø£¶ūĀķĮÖ”¢ĘĻĢŃĢĒČÜŅŗÓėŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ¹²ČČ£¬¶¼»įӊשŗģÉ«³Įµķ²śÉś | |
| D£® | ¹¹³ÉĪļÖŹĪ¢Į£µÄÖÖĄąŗĶŹżĮæ²»Ķ¬”¢±Ė“ĖµÄ½įŗĻ·½Ź½¶ąŃł£¬¾ö¶ØĮĖĪļÖŹµÄ¶ąŃłŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĪŖÓŠŠ§æŲÖĘĪķö²£¬ø÷µŲ»ż¼«²ÉČ”“ėŹ©øÄÉĘ“óĘųÖŹĮ森ӊŠ§æŲÖĘæÕĘųÖŠµŖŃõ»ÆĪļ”¢Ģ¼Ńõ»ÆĪļŗĶĮņŃõ»ÆĪļĻŌµĆÓČĪŖÖŲŅŖ£®
ĪŖÓŠŠ§æŲÖĘĪķö²£¬ø÷µŲ»ż¼«²ÉČ”“ėŹ©øÄÉĘ“óĘųÖŹĮ森ӊŠ§æŲÖĘæÕĘųÖŠµŖŃõ»ÆĪļ”¢Ģ¼Ńõ»ÆĪļŗĶĮņŃõ»ÆĪļĻŌµĆÓČĪŖÖŲŅŖ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


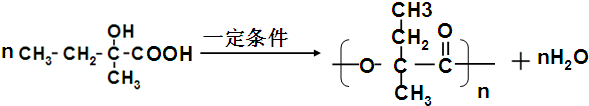
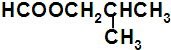 Ӣ
”¢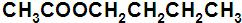 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź¹¼×»ł³Č³ŹŗģÉ«µÄČÜŅŗ£ŗNa+”¢NH4+”¢AlO2-”¢CO32- | |
| B£® | 8% H2O2ČÜŅŗ£ŗH+”¢Fe2+”¢SO42-”¢Cl- | |
| C£® | ŗ¬ÓŠFe3+µÄČÜŅŗ£ŗNa+”¢Al3+”¢Cl-”¢SCN- | |
| D£® | ³ĪĒåĶøĆ÷µÄČÜŅŗÖŠ£ŗCu2+”¢Na+”¢NO3-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢NH4+”¢Cl-”¢SO42- | B£® | Na+”¢H+”¢Cl-”¢CO32- | ||
| C£® | Cu2+”¢K+”¢Cl-”¢NO3- | D£® | K+”¢Ba2+”¢SO42-”¢OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com