
| A. | 0.2molNa2O2 完全与水反应转移的电子数为0.4NA | |
| B. | 800mL 2mol•L-1酒精溶液中所含分子数为0.6NA | |
| C. | 常温常压下,1.6g O2和O3的混合气体所含电子书为0.8NA | |
| D. | 在常温常压下,2.24L NO2与O2混合气体中所含氧原子数为0.2NA |
分析 A.过氧化钠中氧元素的化合价为-1价,1mol Na2O2与水完全反应生成0.5mol氧气,转移了1mol电子;
B.酒精溶液中含酒精分子和水分子;
C.依据n=$\frac{m}{M}$计算氧元素物质的量,计算氧原子中所含电子数分析;
D.在常温常压下,2.24L NO2与O2混合气体物质的量不是0.1mol;
解答 解:A.0.2molNa2O2 完全与水反应,2Na2O2+2H2O=4NaOH+O2,转移的电子数为0.2NA ,故A错误;
B.800mL 2mol•L-1酒精溶液中乙醇物质的量=0.8L×2mol/L=1.6mol,酒精溶液中含酒精分子和水分子,所含分子数大于1.6NA ,故B错误;
C.常温常压下,1.6g O2和O3的混合气体,计算氧元素物质的量得到,氧元素物质的量=$\frac{1.6g}{16g/mol}$=0.1mol,所含电子数=0.1×8×NA=0.8NA,故C正确;
D.在常温常压下,2.24L NO2与O2混合气体物质的量不是0.1mol,混合气体中所含氧原子数不是0.2NA,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的计算应用,物质构成、气体摩尔体积条件应用等知识点,注意酒精溶液中分子包含溶质和溶剂,题目难度中等.


科目:高中化学 来源: 题型:解答题
 对于密闭容器中的反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g)(正反应是放热反应),在673K,30MPa下n(NH3)和n(H2)随时间变化关系如图所示.
对于密闭容器中的反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g)(正反应是放热反应),在673K,30MPa下n(NH3)和n(H2)随时间变化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素、聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 用卤水点豆腐与黄河入海口处沙洲的形成,都体现了胶体聚沉的性质 | |
| C. | 用活性炭为有色物质脱色和用漂白粉漂白有色物质,原理相似 | |
| D. | 为增强84消毒液的消毒效果,使用时可加入浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种气体所含分子数之比为1:1 | |
| B. | 两种气体的摩尔质量之比为1:1 | |
| C. | 两种气体所含原子数之比为1:1 | |
| D. | 两种气体所含的氧原子的摩尔质量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| B | C |
| D |
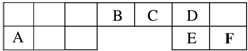
| A. | 简单离子的半径大小关系:C>E | |
| B. | D元素的气态氢化物比C元素的气态氢化物稳定 | |
| C. | 由A、B、C三种元素组成的离子化合物中,阴、阳离子个数比为1:1 | |
| D. | 由C、D、E三种元素组成的化合物,溶液显中性或碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z、E、T、G元素在周期表中的相对位置下表,T的最高价氧化物对水化物有强脱水性,Y和Z在同一周期,Y原子最外层与最内层具有相同电子数.下列判断正确的是( )
X、Y、Z、E、T、G元素在周期表中的相对位置下表,T的最高价氧化物对水化物有强脱水性,Y和Z在同一周期,Y原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | E与G的原子序数相差25 | |
| B. | 常温下,X和Y的单质均能与水剧烈反应 | |
| C. | TE2的熔点高于ZE2晶体 | |
| D. | E、T、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com