
(16分)乙酰水杨酸是一种使用广泛的解热镇痛剂。合成原理是:
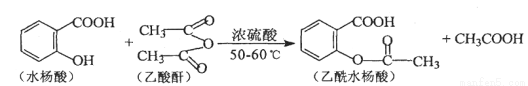
(1)乙酰水杨酸的分子式为 ,1mol乙酰水杨酸最多能与 mol H2 反应。
(2)上面反应的反应类型是 。
(3)有关水杨酸的说法,不正确的是 。
A.能与溴水发生取代反应和加成反应
B.可发生酯化反应和水解反应
C.1mol水杨酸最多能与2mol NaOH反应
D.遇 FeCl3溶液显紫色
(4)乙酰水杨酸与足量KOH溶液反应的化学方程式为 。
(5)乙酰氯(CH3COCl )也可以与水杨酸反应生成乙酰水杨酸,请写出化学反应方程式(不写条 件) 。
(6)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式: 。
Ⅰ.能遇FeCl3溶液显色
Ⅱ.苯环上只有2种一溴取代物
Ⅲ.1mol该化合物能分别与含4mol Br2的溴水或4mol H2 反应
科目:高中化学 来源:2014-2015学年江西省鹰潭市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
[化学—选修3:物质结构与性质](15分)
(1)锌是一种重要的金属,锌及其化合物有着广泛的应用。
①指出锌元素在周期表中的位置: 周期, 族, 区。
②NH3分子中氮原子的杂化轨道类型为 ,基态氮原子的核外电子排布式是 ;
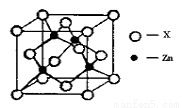
③下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;该化合物的晶体熔点比干冰高得多,原因是 。
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为140-145pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,并阐述理由 。
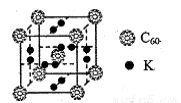
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为 。
③继C60后,科学家又合成了Si60、N60。C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则 Si60分子中的数目为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:填空题
(8分)下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
族 周期 | ⅠA | 0 | |||||||
1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ⑤ | Ne | |||||||
3 | ① | ② | ③ | ④ | ⑥ |
(1)元素④的符号是 ;
(2)⑤和⑥两种元素原子半径的大小关系:⑤ ⑥(填“>”或“<”);
(3)①和②两种元素金属性强弱关系:① ②(填“>”或“<”);
(4)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为: _ ________ _______。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.钠和冷水反应: Na + H2O = Na++OH一+H2↑
B.铁粉投入到硫酸铜溶液中:Fe+Cu2+ =Fe2++Cu
C.AlCl3溶液中加入足量的氨水:Al3++3OH一= Al(OH)3↓
D.氯化亚铁溶液中通入氯气:Fe2+ + Cl2=Fe3+ + 2Cl一
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
下列物质中,属于天然高分子化合物的是
A.蛋白质 B.蔗糖 C.油脂 D.麦芽糖
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三普通高考测试(二)理综化学试卷(解析版) 题型:选择题
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | SO3溶于水后能导电 | SO3为电解质 |
B | 铁比铜活泼 | 铜板上的铁钉在潮湿空气中容易生锈 |
C | 浓H2SO4有强氧化性 | 浓H2SO4常温下能与Cu发生反应 |
D | 小苏打可做焙制糕点的膨松剂 | NaHCO3能与碱反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省揭阳市高三毕业班二模考试理综化学试卷(解析版) 题型:简答题
(16分)查尔酮类化合物是黄酮类药物的主要合成中间体。
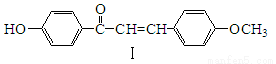
(1)下列查尔酮类化合物I的说法正确的是 。
A.加入溴的四氯化碳溶液,溶液褪色
B.可发生加成或取代反应
C.不与NaOH溶液发生反应
D.加入新制的氢氧化铜有红色沉淀生成
(2)反应①是制取查尔酮类化合物的一种方法:

化合物III的分子式是 ,1mol化合物III最多能与 mol H2发生加成反应。
(3)化合物II可由化合物IV(分子式:C8H10O)在Cu催化氧化下制得,则化合物IV的结构简式为 ,化合物IV的一种同分异构体V为芳香族化合物,其核磁共振氢谱上有四组峰,峰面积之比为为1∶1∶2∶6,则V的结构简式为 (任写一种)。
(4)聚合物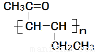 是一种高分子材料,请利用类似反应①方法,用丙烯和丙醛为有机物原料合成该聚合物的单体。合成过程中涉及的反应方程式为 。
是一种高分子材料,请利用类似反应①方法,用丙烯和丙醛为有机物原料合成该聚合物的单体。合成过程中涉及的反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东高考佛山市高三二模理综化学试卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值,下列说法正确的是
A.1mol苯中含有3nA个碳碳双键
B.标准状况下,22.4 L乙烯和丙烯混合气体中所含的分子数目为2nA
C.1mol Cl2与足量Fe粉反应生成FeCl3,转移2nA个电子
D.1L 0.1 mol·L-1 Na2S溶液中含有0.1nA个S2-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高三下学期二模考试理综化学试卷(解析版) 题型:实验题
(14分)某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计使用了如下装置进行实验。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)
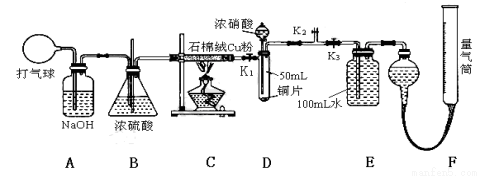
试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是 ;
(2)在铜和浓硝酸反应前,挤压打气球(球内充满空气),经A、B、C反应后,进入D中的气体主要成分
是 (填化学式),通入该气体的目的是 ;进行此步操作时应关闭 ,打开 (填K1、K2或K3)。
(3)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:____ __________。
(4)若E装置中出现倒吸,可采取的应急操作是 ;
(5)从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应 (填“有”或“无”)NO生成。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com