
| A. | 75mL 2mol•L-1氯化镁溶液 | B. | 150mLl 1 mol•L-1氯化钠溶液 | ||
| C. | 50mL3mol•L-1氯化钾溶液 | D. | 50mL 1 mol•L-1氯化铁溶液 |
分析 100ml 1mol•L-1AlCl3溶液中Cl-浓度为1mol/L×3=3mol/L,结合溶质浓度、物质构成计算离子浓度,以此来解答.
解答 解:A.2mol•L-1氯化镁溶液中Cl-浓度为2mol/L×2=4mol/L,故A不选;
B.1 mol•L-1氯化钠溶液中Cl-浓度为1mol/L,故B不选;
C.3mol•L-1氯化钾溶液中Cl-浓度为3mol/L,故C选;
D.1 mol•L-1氯化铁溶液中Cl-浓度为1mol/L×3=3mol/L,故D选;
故选CD.
点评 本题考查物质的量浓度的计算,为高频考点,把握溶质浓度、离子浓度的关系为解答的关键,侧重分析与计算能力的考查,注意离子浓度与溶液体积无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| t/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500 s内N2O5分解速率为2.96×10-3 mol/(L•s) | |
| B. | T1温度下的平衡常数为K1=125,1 000 s时转化率为50% | |
| C. | 其他条件不变时,T2温度下反应到1 000 s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2 | |
| D. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入少量Na固体,平衡逆向移,c(H+)降低 | |
| B. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入少量硫酸氢钠固体,c(H+)增大,Kw不变动 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | |
| B. | 该样品中Cu、O元素的质量比为10:l | |
| C. | V=448 | |
| D. | 溶解样品时消耗H2SO4的物质的量为0.04 mo1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂 | B. | 阿司匹林 | C. | 矿物质 | D. | 维生素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下.22.4L水含有NA个水分子 | |
| B. | 1mol/LNa2C03溶液中含有Na+数目为2NA | |
| C. | 常温常压下,22.4L02中含有2NA个氧原子 | |
| D. | 169O2和O3的混合气体中含氧原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一般地说,K>105时,该反应进行得就基本完全了 | |
| B. | 对一个确定的反应,K值越大,正反应进行的程度越大 | |
| C. | 在温度一定时,K与反应物或生成物的浓度变化无关 | |
| D. | 温度越高,K值越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
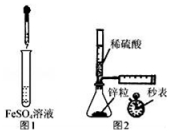
| A. | 制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡 | |
| B. | 测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间 | |
| C. | 中和热测定实验中把盐酸分多次加入氢氧化钠溶液中 | |
| D. | 酸碱中和滴定实验中锥形瓶需要用待测液润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
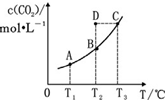 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )| A. | 反应 CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | |
| B. | 在 T2时,若反应处于状态 D,则有 v 正<v 逆 | |
| C. | 平衡状态 A 与 C 相比,平衡状态 A 的 c(CO)小 | |
| D. | 若 T1、T2时的平衡常数分别为 K1、K2,则 K1<K2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com