
| A�� | 1160 | B�� | 2308 | C�� | 1441 | D�� | 2320 |
���� �Ƚ���������ʽ��ӵ� NO2ת��Ϊ�����ķ���ʽ�����ݱ�״����44.8L NO2����ԭ��N2�����������зų�������Ϊ867kJ����a��ֵ��
��� �⣺����������ʽCH4��g��+4NO2��g��=4NO��g��+CO2��g��+2H2O��g����H1=-574kJ•mol-1��CH4��g��+4NO��g��=2N2��g��+CO2��g��+2H2O��g����H2=-akJ•mol-1��ӵã�2CH4��g��+4NO2��g��=2N2��g��+2CO2��g��+4H2O��g����H=-��574+a��kJ•mol-1
�ֱ�״����44.8L NO2����ԭ��N2����2molNO2����ԭ��N2�ų�������Ϊ867kJ������867��2=574+a�����a=1160����ѡ��A��
���� ���⿼���˷�Ӧ�ȵļ����֪ʶ�㣬�������ʵ����������Ĺ�ϵʽ����ų����������ɣ��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | �ζ���Һ����ʼ���� | �ζ���Һ���յ���� |
| 1 | 1.32mL | 23.36mL |
| 2 | 2.26mL | 24.22mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڳ��³�ѹ�£�11.2L N2���еķ�����Ϊ0.5NA | |
| B�� | 32g O2��ԭ����ĿΪ2NA | |
| C�� | ��״���£�18g H2O��ռ�����Ϊ22.4L | |
| D�� | ��ͬ��ͬѹ�£���ͬ����κ����嵥��������ԭ����Ŀ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 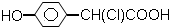 | B�� | CH3CH ��OH��-CH=CH-COOH | ||
| C�� | CH3-CH=CH-COOH | D�� | CH3CH��OH��CH2CHO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
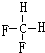 ��
��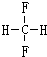
 ��CH2=CH-CH2
��CH2=CH-CH2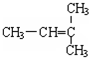 ��
��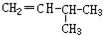
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʪ��ĺ�ɫʯ����ֽ���鰱�� | |
| B�� | ������ͭ��Ũ���ᷴӦ��һ���������� | |
| C�� | �������Ż�ʱ�����ö�����̼�������� | |
| D�� | Na2CO3�����ȶ��Դ���NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ˵����ȷ���ǣ�������
˵����ȷ���ǣ�������| A�� | 1 molA����4 mol Ag��NH3��2OH��Һ����������Ӧ | |
| B�� | �˴Ź�������ͼ��ʾ���������շ� | |
| C�� | ������FeCl3��Һ������ɫ��Ӧ | |
| D�� | 1 mol A����2 mol NaHCO3��ȫ��Ӧ�ų�CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
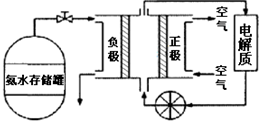
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ��������ԭ�� | B�� | ʹ����ɫΪ��ɫ�Ļ�����Ʒ | ||
| C�� | ��ʹ���κλ�ѧ���� | D�� | ʹ�ò�����������Դ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com