
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源: 题型:
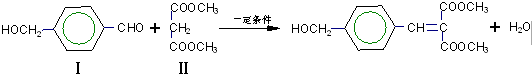
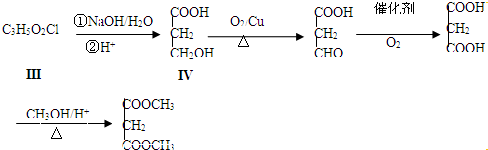
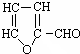 与Ⅱ也能发生类似Ⅰ的knoevenagel反应,则生成有机物结构简式为
与Ⅱ也能发生类似Ⅰ的knoevenagel反应,则生成有机物结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| B、用醋酸溶解水垢中的Mg(OH)2:2H++Mg(OH)2=Mg2++2H2O |
| C、工业上用氨水吸收二氧化硫:2OH-+SO2=SO32-+H2O |
| D、在NaOH溶液中加入少量Ca(HCO3)2溶液:Ca2++2HCO3-+2OH -=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只能为2 | B、可能为2或3 |
| C、只能为4 | D、任意数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
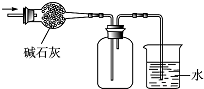
| A、用量筒量取20.00 mL酸性高锰酸钾溶液 |
| B、用蒸发溶剂的方法将10%的氯化铁溶液变为20%的氯化铁溶液 |
| C、用上图的装置可以收集一瓶干燥的氨气 |
| D、可用氯化铁溶液除去试管内壁难以刷去的铜迹 |
查看答案和解析>>
科目:高中化学 来源: 题型:
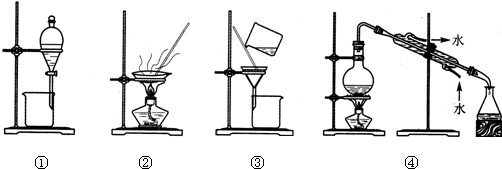
| A、分离乙酸乙酯和碳酸钠溶液,选① |
| B、用CC14提取碘水中的碘,选② |
| C、分离NaCl溶液和沙子,选③ |
| D、用自来水制取蒸馏水,选④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com