
| A. | 500mL溶液中所含K+、SO42-总数为0.3NA | |
| B. | 500mL溶液中含有0.1NA个K+离子 | |
| C. | 1L溶液中K+离子浓度是0.2mol/L | |
| D. | 2L溶液中SO42-离子浓度是0.4mol/L |
分析 A.根据n=cV计算出硫酸钾的物质的量,然后计算出含有K+、SO42-的总物质的量及数目;
B.根据A的计算结果判断;
C.溶液中钾离子浓度与溶液体积大小无关;
D.硫酸根离子浓度与溶液体积大小无关.
解答 解:A.500mL 0.2mol/L K2SO4溶液中含有硫酸钾的物质的量为:0.2mol/L×0.5L=0.1mol,0.1mol硫酸钾中含有0.2mol钾离子、0.1mol硫酸根离子,总共含有0.3mol,所含K+、SO42-总数为0.3NA,故A正确;
B.根据A可知,500mL该溶液中含有0.2mol钾离子,含有0.2NA个K+离子,故B错误;
C.0.2mol/L K2SO4溶液中钾离子浓度为0.4mol/L,钾离子浓度与溶液体积大小无关,则1L溶液中K+离子浓度仍然为0.4mol/L,故C错误;
D.0.2mol/L K2SO4溶液中硫酸根离子浓度为0.2mol/L,2L溶液中SO42-离子浓度不变,仍然为0.2mol/L,故D错误;
故选A.
点评 本题考查物质的量的计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确离子浓度与溶液体积大小无关,为易错点,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
 如图是部分短周期元素的原子序数与其某种常 见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中不正确的有( )
如图是部分短周期元素的原子序数与其某种常 见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中不正确的有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器Ⅰ、Ⅱ中正反应速率相同 | |
| B. | 容器Ⅰ中反应的平衡常数大于容器Ⅲ中反应的平衡常数 | |
| C. | 容器Ⅱ中的气体颜色比容器Ⅰ中的气体颜色深 | |
| D. | 容器Ⅰ中 H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t/min | 0 | 20 | 40 | 60 | 80 | 120 | |
| 第一次试验 | x(HI) | 1 | 0.90 | 0.85 | 0.815 | 0.795 | 0.784 |
| 第二次试验 | x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
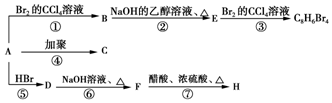
 .
. ,D
,D ,E
,E ,H
,H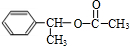 .
. +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr.
+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 米饭、炒肉片、烧带鱼、炒青菜、水果 | |
| B. | 牛奶、炸鸡腿、面包、冰淇淋 | |
| C. | 红烧牛肉、凉拌黄瓜、冬瓜海带汤、烧豆腐 | |
| D. | 馒头、红烧牛肉、清蒸肉圆、骨头汤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com