
【题目】已知pH表示溶液中c(H+)的负对数,同样也可以定义pOH表示溶液中c(OH﹣)的负对数,即pOH=﹣lg(OH﹣),温度T时水的离子积常数用KW表示,则此温度下不能判定溶液呈中性的依据是( )
A.![]() =1
=1
B.pOH= ![]()
C.c(H+)=10﹣pOH
D.pH+pOH= ![]()
 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl36H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有足量的稀硝酸,实验时先打开a并关闭b,用分液漏斗向A中加入过量的盐酸充分反应,此时溶液呈浅绿色;再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl36H2O晶体. 填写下列空白:
(1)滴加盐酸时,发现反应速率较之盐酸与纯铁粉反应要快,其原因是 .
(2)烧杯内放过量稀HNO3的原因是(用离子方程式表示).
(3)整个实验过程中,弹簧夹a都必须打开,除为排出产生的气体外,另一个目的是 .
(4)乙同学对该实验进行了改进,他是用空烧杯盛接滤液,加入适当的试剂,然后在HC1的气流中、一定温度下蒸发、浓缩、降温结晶而得到纯净的FeCl36H2O,你认为加入的试剂可以是 . (填序号) ①适量氯气 ②适量过氧化氢和稀盐酸
③酸性高锰酸钾溶液 ④氢氧化钠溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列反应:
①Fe+CuSO4=Cu+FeSO4 ②CaO+H2O=Ca(OH)2
③Ba(OH)2+H2SO4=BaSO4↓+2H2O ④Zn+2HCl=ZnCl2+H2↑
⑤2KClO3 ![]() 2KCl+3O2↑ ⑥CaCO3
2KCl+3O2↑ ⑥CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
⑦2CO+O2 ![]() 2CO2 ⑧SO 42- +Ba2+=BaSO4↓
2CO2 ⑧SO 42- +Ba2+=BaSO4↓
(1)既是分解反应又是氧化还原反应的是 , 既是化合反应又是氧化还原反应的是(均填序号)
(2)反应①中,氧化剂是;
(3)反应③的离子反应方程式为
(4)写出一个符合⑧的化学反应方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能够大量共存于同一溶液中的是
A.CO32-、H+、Na+、Cl-B.Ag+、Cl-、K+、SO42-
C.K+、OH-、NH4+、NO3-D.Ca2+、Cl-、Na+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列四种溶液:①pH=0的盐酸,②0.1molL﹣1的盐酸,③0.01molL﹣1的NaOH溶液,④pH=11的NaOH溶液中,由水电离生成的H+的物质的量浓度之比为( )
A.1:10:100:1000
B.0:1:12:11
C.14:13:12:11
D.14:13:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。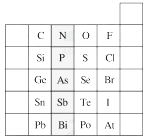
(1)阴影部分元素在元素周期表中的位置为族。
(2)根据元素周期律预测:H3AsO4属于强酸还是弱酸?。
(3)C和Si元素的氢化物都可以燃烧,但Si元素的氢化物在空气中可以自燃,其原因是。试写出Si的氢化物完全燃烧的化学方程式:。
(4)O2与H2的反应是不可逆反应,而S与H2反应有一定限度,请写出Se与H2反应的化学方程式:。
(5)试比较S、O、F三种元素的原子半径大小:(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2 , 而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。 
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应:2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)装置①中发生反应的离子方程式是;
(2)装置②的目的是 , 发生反应的化学方程式是;
(3)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是 ;
(4)实验的具体操作是:先检验装置的气密性,再加入药品,然后(此操作的目的是),最后滴加浓硝酸;
(5)该小组得出的结论所依据的实验现象是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com