
(��7��)��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
�� SO2��2H2O��I2===H2SO4��2HI
�� 2HI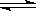 H2��I2
H2��I2
�� 2H2SO4===2SO2��O2��2H2O
��1������������Ӧ�������ж���ȷ����________��
a����Ӧ�����ڳ����½���
b����Ӧ����SO2�����Ա�HIǿ
c��ѭ���������貹��H2O
d��ѭ�����̲���1 mol O2��ͬʱ����1 mol H2
��2��һ���¶��£���1 L�ܱ������м���1 mol HI(g)��������Ӧ��H2���ʵ�����ʱ��ı仯��ͼ��ʾ��
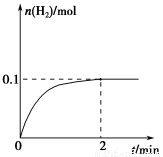
0��2 min�ڵ�ƽ����Ӧ����v(HI)��________�����¶��£�H2(g)��I2(g) 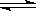 2HI(g)��ƽ�ⳣ��K��________��
2HI(g)��ƽ�ⳣ��K��________��
��ͬ�¶��£�����ʼ����HI(g)�����ʵ�����ԭ����2������________��ԭ����2����
a��ƽ�ⳣ�� b��HI��ƽ��Ũ��
c���ﵽƽ���ʱ�� d��ƽ��ʱH2���������
��3��ʵ������Zn��ϡ������ȡH2����Ӧʱ��Һ��ˮ�ĵ���ƽ��________�ƶ�(����������ҡ�����)�����������������Լ��е�________������H2�����ʽ�����
a��NaNO3 b��CuSO4 c��Na2SO4 d��NaHSO3
��4����H2Ϊȼ�Ͽ���������ȼ�ϵ�ء���֪2H2(g)��O2(g)===2H2O(l) ��H����572 kJ��mol��1ij����ȼ�ϵ���ͷ�228.8 kJ����ʱ������1 molҺ̬ˮ���õ�ص�����ת����Ϊ________��
��1��c ��2��0.1 mol��L��1��min��1 64 b ��3������ b ��4��80%
��������
�����������1���������ڳ������ȶ�����Ӧ�����²�������a�����ɷ�Ӧ���֪����ԭ���Ļ�ԭ�Դ��ڻ�ԭ����Ļ�ԭ�ԣ���ԭ��SO2��HI����SO2�������Ա�HI������b�����ɷ�Ӧ���2+���2+��ɵõ�2H2O�T2H2+O2�����ѭ��������ˮ����Ҫ��ʱ����ˮ��c��ȷ��ѭ�������в���1molO2��ͬʱ����2molH2��d����ѡc����2����ͼ��֪2min�����������ʵ���������0.1mol����������Ũ��Ϊ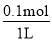 =0.1mol/L����������ʾ�Ļ�ѧ��Ӧ����Ϊ
=0.1mol/L����������ʾ�Ļ�ѧ��Ӧ����Ϊ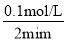 =0.05mol/��L��min����
=0.05mol/��L��min����
�ɷ�Ӧ�еĻ�ѧ��������֪v��HI��Ϊ0.05mol/��L��min����2=0.1mol/��L��min����
2HI��g��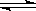 H2��g��+ I2��g��
H2��g��+ I2��g��
��ʼŨ�� 1molL 0 0
ת��Ũ�� 0.2mol/L 0.1mol/L 0.1mol/L
ƽ��Ũ�� 0.8mol/L 0.1mol/L 0.1mol/L
����¶���K1=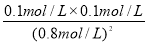 =
=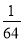 ���� 2HI��g��
���� 2HI��g��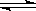 H2��g��+I2��g����H2��g��+I2��g��
H2��g��+I2��g����H2��g��+I2��g��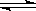 2HI��g����Ϊ�淴Ӧ�������ǵĻ�ѧƽ�ⳣ���ij˻�����1����H2��g��+I2��g��
2HI��g����Ϊ�淴Ӧ�������ǵĻ�ѧƽ�ⳣ���ij˻�����1����H2��g��+I2��g��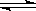 2HI��g���Ļ�ѧƽ�ⳣ��K=
2HI��g���Ļ�ѧƽ�ⳣ��K=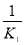 =64���Ը÷�Ӧ�����¶Ȳ��俪ʼ����HI��g�������ʵ�����ԭ����2�������¶Ȳ��䣬K���䣬a�������ʵ���Ϊԭ����2�����÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ����Ӧ��ϵ�и����ʵ�Ũ�ȶ���ԭ����2������b��ȷ�����ʵ���������ѧ��Ӧ����������Ŀ죬����Ũ�ȵļ�С����������ij̶ȱ�С��c�����ɷ�Ӧ����ʽ��ԭ��������������������ȣ�������������½�����ƽ��Ϊ��Чƽ�⣬��ƽ��ʱH2�����������ͬ��d����3����ˮ�ĵ���ƽ��ΪH2O?H++OH-��������������c��H+����ˮ�ĵ������������ã���Zn������H+��c��H+����С��ˮ�ĵ���ƽ�������ƶ���������NaNO3����Һ���������ǿ�����ԣ�����������������NaHSO3���H+��Ӧ������c��H+������Ӧ���ʼ�����Na2SO4 �ļ��룬���Ӳ����뷴Ӧ����Ի�ѧ��Ӧ������Ӱ�죻����CuSO4 ��Zn������ͭ��Һ��Ӧ�û���Cu����ԭ��ؼӿ��˻�ѧ��Ӧ���ʣ���4����2H2��g��+O2��g���T2H2O��I����H=-572KJ/mol��֪������1molˮʱ�ų�������Ϊ572KJ��
=64���Ը÷�Ӧ�����¶Ȳ��俪ʼ����HI��g�������ʵ�����ԭ����2�������¶Ȳ��䣬K���䣬a�������ʵ���Ϊԭ����2�����÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ����Ӧ��ϵ�и����ʵ�Ũ�ȶ���ԭ����2������b��ȷ�����ʵ���������ѧ��Ӧ����������Ŀ죬����Ũ�ȵļ�С����������ij̶ȱ�С��c�����ɷ�Ӧ����ʽ��ԭ��������������������ȣ�������������½�����ƽ��Ϊ��Чƽ�⣬��ƽ��ʱH2�����������ͬ��d����3����ˮ�ĵ���ƽ��ΪH2O?H++OH-��������������c��H+����ˮ�ĵ������������ã���Zn������H+��c��H+����С��ˮ�ĵ���ƽ�������ƶ���������NaNO3����Һ���������ǿ�����ԣ�����������������NaHSO3���H+��Ӧ������c��H+������Ӧ���ʼ�����Na2SO4 �ļ��룬���Ӳ����뷴Ӧ����Ի�ѧ��Ӧ������Ӱ�죻����CuSO4 ��Zn������ͭ��Һ��Ӧ�û���Cu����ԭ��ؼӿ��˻�ѧ��Ӧ���ʣ���4����2H2��g��+O2��g���T2H2O��I����H=-572KJ/mol��֪������1molˮʱ�ų�������Ϊ572KJ��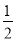 =286KJ�����ص�����ת����ΪΪ
=286KJ�����ص�����ת����ΪΪ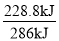 ��100%=80%��
��100%=80%��
���㣺���黯ѧ��Ӧ������ƽ�⡢ȼ�ϵ�ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��һ��ѧ�ڵ����ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ������ѡ���װ�û���������ȷ����
A | B | C | D | |
ʵ�� | �����Ҵ����Ȼ�����Һ | ��ȥˮ�е��Ȼ��� | ����CCl4�е�I2 | ��ȥCO2�����е�HCl���� |
װ�� �� ���� |
|
|
|
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и�һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�������
��14�֣���þ�����Ļ���ﹲ0.2 mol�� ����200 mL 4 mol��L��1��������Һ�У�Ȼ���ٵμ�2mol��L��1��NaOH��Һ����ش��������⣺

��1�����ڵμ�NaOH��Һ�Ĺ����У���������m �����NaOH��Һ�����V�仯�����ͼ��ʾ����V1=160 mLʱ���������ĩ��n (Al)= mol��
��2��0~V1�η����ķ�Ӧ�����ӷ���ʽΪ ��
��3�����ڵμ�NaOH��Һ�Ĺ����У���ʹMg2+��Al3+ �պó�����ȫ�������NaOH��Һ�����V(NaOH)= mL��
��4����þ�����Ļ������Ϊ0.2 mol������þ�۵����ʵ�������Ϊa������200 mL 4mol��L��1�������ܽ�˻������ټ���840mL 2 mol��L��1��NaOH��Һ�����ó�������Al(OH)3����a��ȡֵ��ΧΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и�һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������������۷ֱ��������������NaOH ��Һ��Ӧ��ͬ��ͬѹ�²��������������Ϊ1��1���������NaOH��Һ�����ʵ���Ũ��֮��Ϊ
A��2��3 B��3��1 C��1��2 D��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и߶���ѧ���¿���ѧ�Ծ��������棩 ���ͣ������
(��6��)������(Si3N4)��һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ������У�ͨ�����·�Ӧ�Ƶã�3SiO2(s)+6C(s)+ 2N2(g) 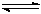 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
��1���÷�Ӧ���������� ��2molN2�μӷ�Ӧת�Ƶ�����Ϊ ��
��2���ﵽƽ��ı�ijһ������������ı�N2��CO����������Ӧ����v��ʱ��t�Ĺ�ϵ��ͼ��
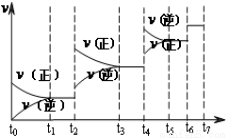
ͼ��t4ʱ����ƽ���ƶ������������� ��ͼ�б�ʾƽ��������CO�ĺ�����ߵ�һ��ʱ���� ��
��3�����÷�Ӧ��ƽ�ⳣ��Ϊ K��729������ͬ�¶���1L�ܱ������У�������SiO2��C��2mol N2��ַ�Ӧ����N2��ת������
(��ʾ��272 = 729)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и߶���ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
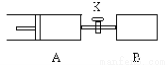
����ͼ����A�г���1molX��1molY����B�г���2molX��2molY����ʼʱA��B�������ȶ�����a L������ͬ�¶Ⱥʹ������ڵ������£��رջ���K��ʹ�������и��Է���������Ӧ��X(g)��Y(g) 2Z(g)��W(g)����H��0��A���ֺ�ѹ��B���ֺ��ݣ���ƽ��ʱ��A�����Ϊ1.4aL������˵���������
2Z(g)��W(g)����H��0��A���ֺ�ѹ��B���ֺ��ݣ���ƽ��ʱ��A�����Ϊ1.4aL������˵���������
A����Ӧ���ʣ�v(B)��v(A) B��A������X��ת����Ϊ80%
C��ƽ��ʱY���������A��B D������K���´�ƽ��VA=2.2aL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и߶���ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��4����Һ����ʵ�飬�±��С������������롰��Һ����Ӧ��ϵ�������
ѡ�� | ���������� | ��Һ |
A | ����Һ�м���KSCN��Һ���۲�������������������ˮ����Һ���ɫ | ���У�e2+��Һ |
B | ����Һ�м������ᣬ����ʹ����ʯ��ˮ����ǵ���ɫ��ζ���� | ����CO32-��Һ |
C | ͨ��CO2����Һ����ǡ��ټ���Ʒ����Һ����ɫ��ȥ�� | ����ΪCa(ClO)2��Һ |
D | ͨ��CO2����Һ����ǣ�����ͨCO2��������������ʧ���ټ�������NaOH��Һ���ֱ���ǡ� | ����ΪCa(OH)2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ�߶���ѧ��1��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�0.1mol��L��1ijһԪ�ᣨHA����Һ��c��OH����/c��H+��=1��10��8������������ȷ����
A����Һ��ˮ�������c��H+��=10��10mol��L��1
B����Һ��c��H+��+c��A����=0.1mol��L��1
C����0.05mol��L��1 NaOH��Һ��������������Һ������Ũ�ȴ�С��ϵΪ��c��A����> c��Na+��> c��OH����> c��H+��
D��ԭ��Һ�м���һ����CH3COONa������ˮϡ�ͣ���Һ��c��OH����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���ɹŰ������и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�����������˵����ȷ����
A��1 mol��������2NA����ԭ��
B��14 g�����к�NA����ԭ��
C��2 L 0.3 mol��L��1Na2SO4��Һ�к�0.6NA��Na��
D��18 gˮ�������ĵ�����Ϊ8NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com