
【题目】下列关于硫及其化合物的说法中,正确的是( )
A. 硫是一种易溶于水的淡黄色晶体
B. 将![]() 通入硝酸酸化的
通入硝酸酸化的![]() 溶液中,有白色沉淀生成,再加盐酸后沉淀消失
溶液中,有白色沉淀生成,再加盐酸后沉淀消失
C. 除去![]() 中混有的
中混有的![]() 、HCl气体可以选用饱和的
、HCl气体可以选用饱和的![]() 溶液
溶液
D. 浓硫酸、浓硝酸、稀硝酸都是氧化性酸,常温下都能使金属铁、铝钝化
【答案】C
【解析】
A.硫是一种淡黄色固体,不溶于水,微溶于酒精,容易溶于CS2,A错误;
B.SO2具有还原性,会被硝酸氧化为硫酸,硫酸与溶液中的BaCl2发生反应产生BaSO4,BaSO4既不溶于水,也不溶于酸,B错误;
C.SO3与水反应产生H2SO4,硫酸与饱和的NaHSO3溶液发生反应产生SO2气体,HCl溶于水,也会与溶液中的NaHSO3发生反应产生SO2气体,达到除杂净化的目的,C正确;
D.浓硫酸、浓硝酸、稀硝酸都是氧化性酸,但在常温下,浓硫酸、浓硝酸可将Fe、Al表面氧化产生一层致密的氧化物薄膜,阻止金属的进一步氧化,即能使金属铁、铝钝化,而稀硝酸与Fe、Al会发生剧烈反应,不会产生钝化现象,D错误;
故合理选项是C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质结构与性质)
镍及其化合物在工业生产和科研领域有重要的用途。请回答下列问题:
(1)基态 Ni 原子中,电子填充的能量最高的能级符号为______,价层电子排布式为________。
(2)Ni(CO)4 常用作制备高纯镍粉,其熔点为-19.3 ℃, 沸点为 43 ℃。则:
①Ni(CO)4 的熔、沸点较低的原因为________。
②写出一种与CO 互为等电子体的分子的化学式________。
③Ni(CO)4中 σ 键和 π 键的数目之比为________。
(3)NiSO4 常用于电镀工业,其中 SO42-的中心原子的杂化轨道类型为________,该离子中杂化轨道的作用是________。
(4)氧化镍和氯化钠的晶体结构相同,可看成镍离子替换钠离子,氧离子替换氯离子。 则:
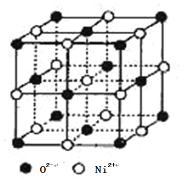
①镍离子的配位数为________。
②天然的和人工合成的氧化镍常存在各种缺陷,某缺陷氧化镍的组成为Ni0.97O(相对分子质量为73), 其中 Ni 元素只有+2 和+3 两种价态, 两种价态的镍离子数目之比为________;若阿伏加德罗常数的值为NA,晶体密度为 ρ g·cm-3,则该晶胞中最近的 O2-之间的距离为________pm(列出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明的强酸性溶液中,能大量共存的一组离子是
A. Mg2+、A13+、SO42-、NO3- B. Na+、HCO3-、K+、SO42-
C. MnO4-、K+、SO42-、Na+ D. NH4+、Fe2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1LFeBr2溶液中,通入1.12L(标态下)的Cl2,测得溶液中c(Br-)=3c(Cl-),反应过程中溶液的体积变化不计,则下列说法中正确的是
A. 原溶液的浓度为0.1mol/L B. 反应后溶液中c(Fe3+)=0.1mol/L
C. 反应后溶液中c(Fe3+)=c(Fe2+) D. 原溶液中c(Br-)=0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象所对应的离子方程式不正确的是( )
选项 | 实验 | 现象 | 离子方程式 |
A | 将稀硫酸滴加到KI淀粉溶液中 | 在空气中放置一段时间后溶液呈蓝色 |
|
B | 用硫氰化钾溶液检验某溶液中含有 | 溶液变成红色 |
|
C | 酸性 | 溶液紫色褪去 |
|
D | 将 | 有白色沉淀生成 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是
A.Cu2+、Mg2+、SO42-、OH-B.Na+、H+、SO42-、ClO-
C.MnO4-、Al3+、Fe2+、SO42-D.Na+、NO3-、K+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有______性.
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:2KClO3+SO2==2ClO2+_____。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,写出化学方程式:_____________
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg/L之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2== S4O62-+2I-)
Ⅲ加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:

请回答:
①操作Ⅰ中反应的离子方程式是_____。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是_____。
③若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mol/L的Na2S2O3溶液10ml,则水样中ClO2的浓度是_____ mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某有机化合物A的结构及性质,进行如下实验:
I.确定分子式
(1)将有机物A置于氧气流中充分燃烧实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下),则A中各元素的原子个数比为______________。
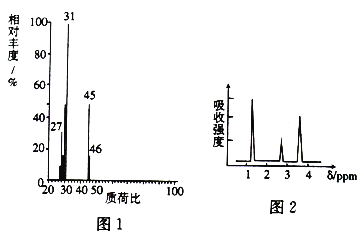
(2)A的质谱图如图1所示,则A的分子式为_____________。
II.结构式的确定
(3)经测定,A的核磁共振氢谱图如图2所示,则A的结构简式为____________。
III.性质实验
(4)A在一定条件下可脱水生成无色气体B,该反应的化学方程式为____________。
(5)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉。制备氯乙烷的一个好方法是用A与SOCl2加热下反应,同时生成二氧化硫和氯化氢两种气体,则该反应的化学方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com