
����Ŀ�����������Ҫ�ɷ���Al2O3 �� ��������SiO2��Fe2O3��MgO����ҵ�ϴ�����������ȡ���ɲ�����ͼ��ʾ�������̣� 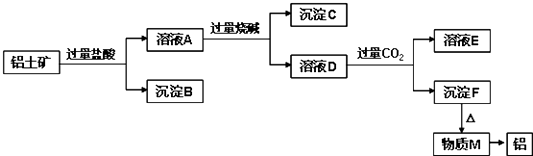
��ش��������⣺
��1��ͼ���漰������Һ�������ʵ�鷽��������������ƣ�����Ҫ�õ��IJ��� ��������
��2������B�ijɷ������ѧʽ����ͬ��������C�ijɷ�������
��3��д��������ҺD�����ӷ���ʽ��
��4������Fת��Ϊ����M�Ļ�ѧ����ʽΪ����ҺD��ͨ�����CO2���ɳ���F�����ӷ���ʽΪ ��
���𰸡�
��1�����ˣ��ձ�����������©��
��2��SiO2��Mg��OH��2��Fe��OH��3
��3��Al3++4OH��=AlO2��+2H2O
��4��2Al��OH��3 ![]() Al2O3+3H2O��AlO2��+CO2+2H2O=Al��OH��3��+HCO3��
Al2O3+3H2O��AlO2��+CO2+2H2O=Al��OH��3��+HCO3��
���������⣺Al2O3��SiO2��Fe2O3��MgO�У�Al2O3��SiO2��NaOH��Һ��Ӧ��MgO��Fe2O3����NaOH��Һ��Ӧ����SiO2�������ᷴӦ�⣬Al2O3��Fe2O3��MgO�������ᷴӦ������������ᣬ��ҺAΪAlCl3��MgCl2��FeCl3 �� ����BΪSiO2 �� ��������ռ����CΪFe��OH��3��Mg��OH��2 �� ��ҺDΪNaAlO2 �� ͨ�����������̼����ҺEΪNaHCO3 �� ����FΪAl��OH��3 �� ���ȷֽ�õ�MΪAl2O3 �� �����ɵõ�Al����1��������Һ�������ʵ�鷽���ǹ��ˣ����õ���ʵ���������ձ�����������©�������Դ��ǣ����ˣ� �ձ�����������©������2�������Ϸ�����֪����B�ijɷ���SiO2 �� ����CΪFe��OH��3��Mg��OH��2 �� ���Դ��ǣ�SiO2�� Mg��OH��2��Fe��OH��3����3����ҺDΪNaAlO2 �� ���ɵ����ӷ���ʽΪAl3++4OH��=AlO2��+2H2O�����Դ��ǣ�Al3++4OH��=AlO2��+2H2O����4������Fת��Ϊ����M�Ļ�ѧ����ʽΪ2Al��OH��3 ![]() Al2O3+3H2O����ҺNaAlO2��ͨ�����CO2����Al��OH��3��������Ӧ�����ӷ���ʽΪCO2+AlO2��+2H2O�TAl��OH��3��+HCO3�� ��
Al2O3+3H2O����ҺNaAlO2��ͨ�����CO2����Al��OH��3��������Ӧ�����ӷ���ʽΪCO2+AlO2��+2H2O�TAl��OH��3��+HCO3�� ��
���Դ��ǣ�2Al��OH��3 ![]() Al2O3+3H2O��AlO2��+CO2+2H2O=Al��OH��3��+HCO3�� ��
Al2O3+3H2O��AlO2��+CO2+2H2O=Al��OH��3��+HCO3�� ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڱ�����������ȷ���ǣ� ��
A. ����Ҫ����ʯ��Ϊԭ�϶���õ�һ����Ҫ����ԭ��
B. ���к���̼̼˫�������Ա�����ϩ��
C. ��������6��̼̼��ѧ����ȫ��ͬ
D. ����������ˮ�����������Һ��Ӧ��ʹ������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ��ȥCO2�к��е�������SO2���ʣ���ѡ�õ�һ���Լ���( )
��NaOH��Һ ��NaHCO3��Һ ��Na2CO3��Һ
��HNO3�ữ��Ba(NO3)2��Һ ����ˮ ������KMnO4��Һ
A. �ڢ�B. �ڢ�C. �ڢܢ�D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��D��E��F��G���ֶ����ڵ�����Ԫ�أ�A��ԭ�Ӱ뾶��С��B����������������������������2����B��D�г��ȼ����������ۻ�����BD2 �� E+��D2��������ͬ�ĵ��Ӳ�ṹ��G��Dͬ���壬A������F������ȼ�յIJ�������ˮ�õ�һ��ǿ��X����ش��������⣺
��1��BD2�ĽṹʽΪ ��
��2��GԪ����Ԫ�����ڱ��е�λ��Ϊ �� ��GD2���������Ƶ�F���ʵ�ˮ��Һ�����ӷ���ʽΪ ��
��3�������Ԫ���к�AԪ�صĶ�Ԫ���ӻ�����ĵ���ʽΪ �� D��E�γɵĻ��������DZˮ����еĹ���������û�������ˮ��Ӧ�����ӷ���ʽΪ ��
��4��A��B��D��Ԫ������ɵ�ijһԪ��Y���ճ������г�����һ�ֵ�ζ�����ڵ������Ũ�ȵ�X��Y��Һ�м�����״��ͬ��������п�������ߵ�ƽ����Ӧ���ʵĴ�С��ϵ��XY�������������=������
��5����A��D��E��G��Ԫ�ؿ��γ�������ʽ�Σ�����������ʽ����ˮ��Һ�з�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3��Һ������ӡˢ��·ͭ��ĸ�ʴ�����ø�ʴ���̵����ӷ���ʽΪ �� �����÷�Ӧ��Ƴ�ԭ��أ�������ͼ�����л���ԭ��ص�װ�ü�ͼ����������������������Ϻ͵������Һ�� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��Ӧ����C���ٶ���Ӧ��A��B��ʼ�����ǵ���ʼŨ�Ⱦ�Ϊ1mol/L����Ӧ����2min��A��Ũ��Ϊ0.8mol/L��B��Ũ��Ϊ0.6mol/L��C��Ũ��Ϊ0.6mol/L����2min�ڷ�Ӧ��ƽ������VB= �� �÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ģ��ϳɰ��Ͱ����������������£�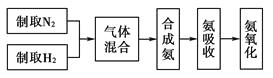
��֪ʵ���ҿ��ñ�����������(NaNO2)��Һ�뱥���Ȼ����Һ�����Ⱥ�Ӧ��ȡ������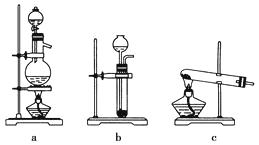
��1������ͼ��ѡ����ȡ����ĺ���װ�ã�������������
��2������������ͨ����װ�ã���װ�õ����ó��˽��������⣬��������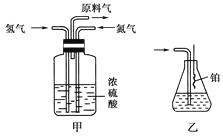
��3�����ϳ�����������ȴ����������ͨ����װ�õ�ˮ�����հ���(���ᡱ���ᡱ)����������ԭ������
��4������װ������һ��ʱ�䰱����ͨ�������ͬʱ�����ȵIJ�˿������װ�õ���ƿ�ڣ���ʹ��˿���ֺ��ȵ�ԭ���� ��
��ƿ�л��ɹ۲쵽����������
��5��д����װ���а������Ļ�ѧ����ʽ����
��6����Ӧ��������ƿ�ڵ���Һ�к���H����OH��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������D��һ�ֺ�ɫ����� 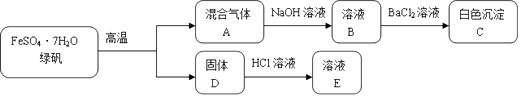
��1���������Aͨ������NaOH��Һ����ҺB�������ε������� ��
��2����ɫ����C�м��������ʵ������Ϊ ��
��3������D��HCl��Һ��Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com