
| A��ԭ�������ͭ������0.15mol |
| B��ϡ��������ʵ�����Ũ��Ϊ2mol��L-1 |
| C����һ��ʣ��4.8g����Ϊͭ |
| D���ټ�������ϡ���ᣬ�ֵõ���״����6.72LNO |
| 2 |
| 3 |
| 2.24 |
| 22.4 |
| 0.4mol |
| 0.2L |
| 1 |
| 3 |


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
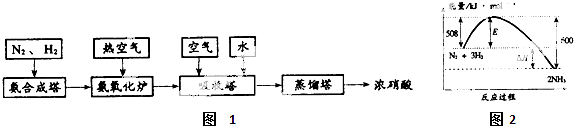
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��60% | B��40% |
| C��24% | D��4% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
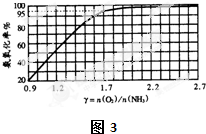
 ����ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⣮ij�о�С����ʵ������Ag-ZSM-5 Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�����ͼ��
����ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⣮ij�о�С����ʵ������Ag-ZSM-5 Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�����ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1.5mol?L-1 |
| B��2mol?L-1 |
| C��2.5mol?L-1 |
| D��3mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ�������Cu��O�����ʵ���֮��Ϊ2��1 |
| B����������ʵ���Ũ��Ϊ2.6mol/L |
| C��������NO�ڱ�״���µ����Ϊ4.48L |
| D��Cu��CuO��Cu2O�����ᷴӦ��ʣ��HNO3Ϊ0.2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4 C2H8 |
| B��C2H4 C2H2 |
| C��C2H2 C2H6 |
| D��CH4 C2H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������������ʱ�������¶ȿ���ʹƽ������ȷ�Ӧ�����ƶ� |
| B����������������ʱ��ʹ�ô���ֻ�ܸı䷴Ӧ���ʣ�������ʹ��ѧƽ���ƶ� |
| C�����ݻ��ɱ�������г����뷴Ӧ�ص����壬ƽ��һ�����ƶ� |
| D����������������ʱ������ѹǿһ�����ƻ����巴Ӧ��ƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ӦΪ4OH--4e-=2H2O+O2�� |
| B���ŵ�ʱCO32-���ƶ� |
| C��������1 molˮʱ��ת��4 mol���� |
| D��ͨH2��һ��Ϊ������������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com