
【题目】某小组同学利用下图装置对电解氯化铜实验进行了研究。
装置 | 现象 |
| 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,烧杯壁变热,溶液由蓝色变为绿色 |
(1)甲认为电解过程中阳极产生的_________是溶液变绿的原因。
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2+ + 4Cl-![]() [CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:________________。
[CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:________________。
(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
装置 | 现象 |
| 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色;U型管变热,冷却后阴极附近溶液仍为绿色 |
丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依据是________,否定乙的依据是________________。
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]-,[CuCl2]-掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]-的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]-掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]-的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是__________________。
② 写出b中生成[CuCl2]-的离子方程式:____________________。
③ 补充c中必要的操作及现象:____________________。
丙据此得出结论:电解时阴极附近生成[CuCl2]-是导致溶液变绿的原因。
【答案】 Cl2 电解过程放热导致温度升高,Cu2+ + 4Cl-![]() [CuCl4]2-正向移动 阳极附近溶液仍为蓝色 U型管冷却后阴极附近溶液仍为绿色 证明在上述实验条件下,电解后的绿色溶液中存在[CuCl2]- Cu2+ + 4Cl-+ Cu
[CuCl4]2-正向移动 阳极附近溶液仍为蓝色 U型管冷却后阴极附近溶液仍为绿色 证明在上述实验条件下,电解后的绿色溶液中存在[CuCl2]- Cu2+ + 4Cl-+ Cu ![]() 2[CuCl2]- 加入CuCl2蓝色溶液,直至溶液颜色与电解后绿色溶液基本相同
2[CuCl2]- 加入CuCl2蓝色溶液,直至溶液颜色与电解后绿色溶液基本相同
【解析】(1) 用石墨作阴阳极,电解CuCl2溶液,阳极石墨上析出氯气,氯气呈黄绿色,能溶于水,使水溶液呈绿色。正确答案为氯气(或Cl2)。
(2)在CuCl2溶液中存在平衡:Cu2+ + 4Cl— ![]() [CuCl4]2— (黄色) ΔH>0,根据实验现象,电解后烧杯壁变热,说明温度升高了,使该平衡向正反应方向移动,使[CuCl4]2—浓度增大。
[CuCl4]2— (黄色) ΔH>0,根据实验现象,电解后烧杯壁变热,说明温度升高了,使该平衡向正反应方向移动,使[CuCl4]2—浓度增大。
(3)丙的实验证明电解后在阳极上仍有氯气产生,但阳极附近的溶液没有变绿色,仍是蓝色,所以否定了甲;而阴极上有红色物质析出,溶液由蓝色变绿色,U型管变热,这些现象与乙的相同,但是冷却后溶液仍为绿色,可见,温度的改变并没有改变溶液的颜色,也就是说上述平衡没有受温度的改变而移动,所以否定了乙。
(4) ①根据资料“ii :稀释含[CuCl2]—的溶液生成CuCl白色沉淀”。所以a操作的目的就是证明上述实验,电解后的绿色溶液中含[CuCl2]-;② 根据b叙述中涉及到的物质,即可写出反应的离子方程式为Cu2+ + 4Cl-+ Cu![]() 2[CuCl2]- 。③根据资料“i:[CuCl2]—掺杂Cu2+后才呈黄色”,所以c的操作就是加入CuCl2溶液,直至溶液也呈绿色,再重复操作a,有白色沉淀生成,证明绿色溶液中确实含有[CuCl2]—。
2[CuCl2]- 。③根据资料“i:[CuCl2]—掺杂Cu2+后才呈黄色”,所以c的操作就是加入CuCl2溶液,直至溶液也呈绿色,再重复操作a,有白色沉淀生成,证明绿色溶液中确实含有[CuCl2]—。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】萜类化合物是天然物质中最多的一类物质,有些具有较强的香气和生理活性。某些萜类化合物可以相互转化。下列说法错误的是
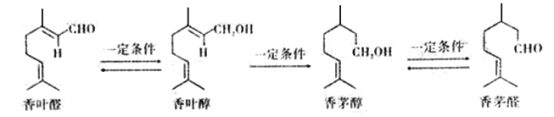
A. 香叶醛的分子式为C10H16O
B. 香叶醇和香茅醛互为同分异构体
C. 上述四种物质均能使酸性高锰酸钾溶液或溴水褪色
D. 香茅醇可以发生取代反应加成反应及氧化反应,但是不能发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.1 mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述正确的是
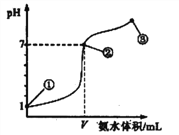
A. V=20mL
B. 在点①所示溶液中:c(Cl-)=c(H+)
C. 在点②所示溶液中:c(H+)=c(NH3·H2O)+c(OH-)
D. 在点②、③之间可能存在:c(NH4+)>c(Cl-)=c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氧化二钒在工业生产中有重要用途。某含钒废料的成分为V2O5、V2O4、SiO2、Fe2O3、Al2O3,实验小组从其中回收V2O5的一种工艺流程如下:
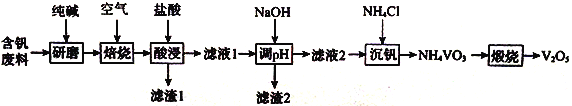
请回答下列问题;
(1)(研磨)的目的为__________________。所加纯碱不宜过量太多,理由为_________。
(2)“焙烧”后所得混合物中除含Na2CO3、NaVO3、Fe2O3、NaA1O2外,还含有________(填化学式)。
(3)“酸浸”时,VO3-转化为VO2+,转化反应的离子方程式为_________________________;滤渣1的主要成分为_________________(填化学式)。
(4)已知:常温下,Al(OH)3、Fe(OH)3 饱和溶液中金属阳离子浓度的负对数[-lg c(M3+ )]与pH 的关系如图所示:
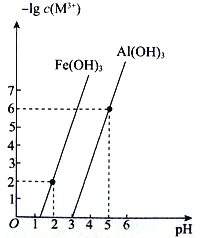
常温下,Ksp[Fe(OH)3]=________________________;当调pH=4 时,溶液中A13+________(填“是”或“否”)沉淀完全。(已知;溶液中离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全)
(5)“煅烧”时,反应的化学方程式为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。
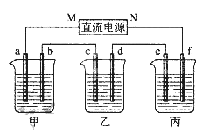
接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
(1)电源的N端为________极;
(2)电极b上发生的电极反应为:__________________,生成的气体在标准状况下的体积为__________L(保留两位有效数字);
(3)若要使乙溶液恢复到电解前的状态,可向乙溶液中加入________(填化学式),质量为________g(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白铁皮在发生析氢腐蚀时有0.2mol电子转移,下列说法正确的是( )
A. 有5.6 g金属被腐蚀
B. 有6.5 g金属被氧化
C. 有0.15 mol金属失去电子
D. 标准状况下有4.48 L H2逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、请用勒·夏特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。_______________________________________________________________
II、一密封体系中发生下列反应:N2 +3H2 ![]() 2NH3 +Q,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 +Q,下图是某一时间段中反应速率与反应进程的曲线关系图:

回答下列问题:
(1)处于平衡状态的时间段是_______________________
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化?____________、 ____________、____________
(3)下列各时间段时,氨的百分含量最高的是(______)
A、t0~t1 B、t2~t3 C、t3~t4 D、t5~t6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,在H2C2O4、NaOH混合溶液中,c(H2C2O4)-c(HC2O4-)+c(C2O42-)=0.100mol/L。含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。下列说法正确确是
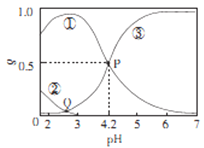
A. ①表示H2C2O4的分布曲线,③表示C2O42-的分布曲线
B. 20℃时,H2C2O4的二级电离平衡常数Ka=1×10-4.2
C. Q点对应溶液中lgc(H+)<lgc(OH-)
D. 0.100mol/L的NaHC204溶液中:c(OH-)=c(H+)-2c(C2042-)+c(H2C2O4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com