
用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是 ( )
A.CuCl2(CuCl2溶液) B.AgNO3(Ag2O) C.NaCl(HCl溶液) D.CuSO4(Cu(OH)2)
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源:2013-2014浙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列说法错误的是
A.0.1mol某醛与足量的银氨溶液反应,产生银的质量为21.6g,则该醛肯定为二元醛
B.乙醇、苯酚、乙酸都有羟基,但是电离常数不同,这主要是基团之间相互影响造成的
C. 分子中最多19个碳原子共平面、最多6个原子共直线
分子中最多19个碳原子共平面、最多6个原子共直线
D.分子式为C10H20O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C,则有机物A的可能结构有4种
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:填空题
某稀硫酸和硝酸的混合溶液200 mL,分成两份。向其中一份逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO)。向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如下图所示。

(1)第二份溶液中最终溶质为 ;
(2)OA段产生的气体是 (填化学式),BC段产生的气体是 (填化学式),AB段的反应为 ;
(3)原混合酸中HNO3的物质的量为 mol,H2SO4的物质的量浓度应为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
下图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述正确的是

A.A气体是CO2,B气体是NH3
B.第Ⅲ步得到的晶体是Na2CO3·10H2O
C.第Ⅱ步的离子方程式为Na++NH3·H2O+CO2===NaHCO3↓+NH
D.第Ⅳ步操作的主要过程有溶解、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
催化剂是化工技术的核心,绝大多数的化工生产均需采用催化工艺。
(1)人们常用催化剂来选择反应进行的方向。下左图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。

①在有催化剂作用下,CH3OH与O2 反应主要生成 (填“CO、CO2、HCHO”);
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g) △H= 。
(2)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O=2n CuSO4+(2-2n) H2SO4
从环境保护的角度看,催化脱硫的意义为 ;每吸收标准状况下11.2L SO2,被SO2还原的O2的质量为 g。
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式 。

查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有关电化学原理的说法错误的是( )
A.氯化铝的熔点比氧化铝低,因此工业上最好采用电解熔融氯化铝来制备单质铝
B.电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极
C.对于冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法
D.对大型船舶的外壳进行的“牺牲阳极的阴极保护法”,是应用了原电池原理
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列关于教材中的各项说法错误的一项是( )
A.在化学反应中,反应物转化为生成物的同时,必然发生能量的变化
B.氮肥包括铵态氮肥、硝态氮肥和尿素
C.在书写热化学方程式时应标明反应物及生成物的状态,无需标明反应温度和压强
D.医疗上用的石膏绷带是利用熟石膏与水混合成糊状后很快凝固的性质
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省台州市路桥区高考理综化学模拟试卷一试卷(解析版) 题型:推断题
(15分)某有机物X(C13H14O8)分子中含有多种官能团,其结构为(其中I、II为未知部分的结构):

为推测X的分子结构,现进行如图所示的转化。

已知:①E分子中检测到18O原子,向E的水溶液中滴入FeCl3溶液显紫色,E的核磁共振氢谱中有4组峰,且峰面积之比为1︰2︰2︰1,E与NaHCO3反应有CO2产生;②G的分子式为C2H2O4。请回答下列问题:
(1)E分子所含官能团的名称是 _________________ ;X溶液遇FeCl3溶液不显紫色,则X的结
构简式为 __________________________________ 。
(2)写出B与G反应生成M(分子内含有六元环)的化学方程式:_____________________ 。
(3)F有特殊愉快的酸味,可作为食品饮料的添加剂;F的聚合物具有良好的生物相容性,可作为手术缝合线等材料广泛应用于生物医药和生物材料领域。由B经过下列途径可合成F:

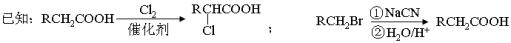
①N→T的反应类型是 __________ ,N的结构简式是 _____________ 。
②写出T→F的第一步反应的化学方程式: ___________________________________ 。
(4)E有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:_____________ 。
①属于芳香族化合物;②能发生银镜反应;③苯环上的一氯代物只有2种
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:选择题
有机物的化学性质主要由其官能团决定。苹果酸是一种有机酸,结构简式为:
 。下列有关苹果酸的说法不正确的是
。下列有关苹果酸的说法不正确的是
A.1mol苹果酸足量金属钠反应,生成氢气3g
B.1mol苹果酸与足量氢氧化钠溶液反应,消耗3 mol氢氧化钠
C.1mol苹果酸能与足量的碳酸氢钠溶液反应,标况下生成44.8L的二氧化碳气体
D.苹果酸在一定条件下既能与醋酸反应,又能与乙醇反应,也可以自身发生酯化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com