
| A. | 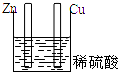 | B. | 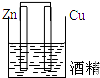 | C. | 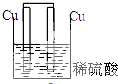 | D. | 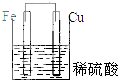 |
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸雨是指pH<5.6雨 | |
| B. | 在正常情况下人体血液pH为7.35~7.45 | |
| C. | 有色水泥主要是因为水泥中含有CuCl2 | |
| D. | 红色玻璃主要是因为玻璃中含有少量Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列关于DDT的说法中正确的是:( )
,下列关于DDT的说法中正确的是:( )| A. | DDT分子中两苯环不可能共平面 | |
| B. | DDT分子属于芳香烃 | |
| C. | 若使原苯环上的两个氯原子连接在同一个苯环上,共有6种同分异构体 | |
| D. | DDT难以降解的原因是DDT难以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1):P-P:198,P-O:360,O=O:498,则1mol白磷发生反应:P4(白磷)+3O2═P4O6的热效应为( )
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或断开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1):P-P:198,P-O:360,O=O:498,则1mol白磷发生反应:P4(白磷)+3O2═P4O6的热效应为( )| A. | 放出1 638 kJ的热量 | B. | 吸收1 638 kJ的热量 | ||
| C. | 放出126 kJ的热量 | D. | 吸收126 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O.
 、
、 、
、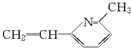 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热,须看反应物和生成物所具有的总能量的相对大小 | |
| D. | 金刚石比石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
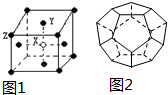 (1)下列4种物质熔点沸点由高到低排列为①>④>③>②(填序号)
(1)下列4种物质熔点沸点由高到低排列为①>④>③>②(填序号)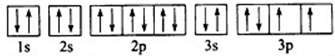 .其最高价氧化物对应的水化物的化学式是H2SO4.
.其最高价氧化物对应的水化物的化学式是H2SO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com