
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:分析 I.(1)元素的金属性越强,其单质与酸反应越剧烈;根据电子转移守恒,金属失去电子越多生成氢气体积越大;
(2)氯气具有强氧化性,能将硫离子氧化为S单质;
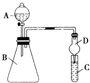
II.(1)根据仪器的结构特征,可知出仪器B为锥形瓶;球形干燥管具有防止倒吸的作用;
(2)氯气具有强氧化性,能将碘离子氧化为碘单质,碘遇淀粉试液变蓝色;氯气有毒,不能直接排空,但能和碱溶液反应生成盐.
解答 解:Ⅰ.(1)Na与K同主族,K的金属性比Na的强,钠、镁、铝为同周期金属元素,金属性依次减弱,故钾与盐酸反应最剧烈,铝与盐酸反应最缓慢;根据得失电子守恒,失去的电子数越多,产生的气体越多,故铝与盐酸反应生成的氢气最多,
故答案为:钾;铝;铝;
(2)氯气具有强氧化性,氯气和Na2S反应生成NaCl和单质硫,离子方程式为:S2-+Cl2═S↓+2Cl-,
故答案为:S2-+Cl2═S↓+2Cl-;
Ⅱ.(1)B仪器名称是锥形瓶,干燥管上部空间大,有缓冲作用,能防止倒吸现象,
故答案为:锥形瓶;倒吸;
(2)KMnO4与浓盐酸反应生成氯气,氯气与淀粉碘化钾混合溶液反应生成碘单质,碘遇淀粉试液变蓝色,氯气作氧化剂、碘是氧化产物,所以氧化性:氯气>碘,则非金属性:Cl>I,过量的氯气会逸散到空气中,污染环境,可用碱液吸收,
故答案为:变蓝;NaOH.
点评 本题考查了实验方案设计,涉及金属、非金属性强弱的探究,明确物质的性质是解本题关键,同时考查学生灵活运用知识解答问题的能力,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 物质 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ②HNO3 | ③NaOH、KOH或NH3•H2O ④Ba(OH)2 | ⑤Na2CO3 ⑥NaNO3、Na2SO4或NH4NO3 | ⑦CO2 ⑧Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
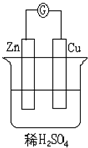 如图,请读题并填空:在图中,
如图,请读题并填空:在图中,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将一定质量的镁铝合金投入200mL 一定浓度的盐酸中,合金完全溶解.
将一定质量的镁铝合金投入200mL 一定浓度的盐酸中,合金完全溶解.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气中的SO2溶于水,最终形成酸雨 | |
| B. | 汽车排放的尾气、硝酸厂和化肥厂的废气都含有氮氧化物 | |
| C. | 工业废水任意排放是造成酸雨的主要原因 | |
| D. | 为了减少酸雨的形成,必须减少SO2的排放量,对燃料脱硫处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 水和干冰的气化 | D. | 氯化钠和氯化氢溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
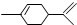 ),下列有关它的推测不正确的是( )
),下列有关它的推测不正确的是( )| A. | 分子式为C10H16 | |
| B. | 常温下呈液态难溶于水 | |
| C. | 所有原子可能共平面 | |
| D. | 与过量溴的CCl4 溶液反应后产物(如图)为: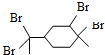 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验氯乙烷中的氯元素,加碱溶液加热后,用稀硫酸酸化后,再检验 | |
| B. | 鉴别溶液中是否有SO42-,用盐酸酸化 | |
| C. | 为抑制Fe2+的水解,用稀硝酸酸化 | |
| D. | 为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 污 染 指 数 | 首要 污染物 | 空气 质量等级 | ||
| SO2 | NO2 | PM10 | ||
| 23 | 35 | 56 | PM10 | 良 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com