
分析 (1)①依据配制一定物质的量浓度溶液的一般步骤选择需要的仪器,判断缺少的仪器,注意容量瓶规格选择应依据配制溶液体积;
②依据配制一定物质的量浓度溶液的一般步骤排序;
(2)依据m=CVM计算需要溶质的质量;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(4)二氧化硅与氢氧化钠溶液反应生成具有粘性的硅酸钠溶液,能够将玻璃塞与玻璃瓶粘到一起.
解答 解:(1)①配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管,配制NaOH溶液480mL,应选择500mL容量瓶,所以缺少的仪器:500 mL容量瓶、胶头滴管;
溶质溶解冷却后,应将溶液转移到500mL容量瓶,定容时继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
故答案为:500 mL容量瓶、胶头滴管;
②配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,所以正确的操作顺序为:a b d c f e;
(2)配制物质的量浓度为1mol•L-1的NaOH溶液480mL,应选择500mL容量瓶,实际配制500mL溶液,需要氢氧化钠质量m=1mol/L×0.5L×40g/mol=20.0g;
故答案为:20.0;
(3)A.溶解固体溶质时,未冷却至室温即转入容量瓶进行定容,冷却后,溶液体积偏小,溶液浓度偏高,故A选;
B.定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故B不选;
C.容量瓶中原有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故C不选;
D.定容时观察液面仰视,导致溶液体积偏大,溶液浓度偏低,故D不选;
故选:A;
(4)二氧化硅与氢氧化钠溶液反应生成具有粘性的硅酸钠溶液,能够将玻璃塞与玻璃瓶粘到一起,化学方程式:SiO2+2NaOH=Na2SiO3+H2O;
故答案为:SiO2+2NaOH=Na2SiO3+H2O.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意误差分析的方法和技巧,题目难度不大.


科目:高中化学 来源: 题型:选择题
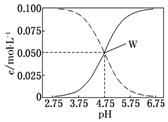 常温下,醋酸、醋酸钠混合溶液中,已知c(CH3COOH)+c(CH3COO-)=0.1mol•L-1,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的说法正确的是( )
常温下,醋酸、醋酸钠混合溶液中,已知c(CH3COOH)+c(CH3COO-)=0.1mol•L-1,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的说法正确的是( )| A. | pH=5.75的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | pH=7,c(Na+)=0.1 mol•L-1,c( CH3COOH)>c(Na+)=c( CH3COO-)>c(H+)=c(OH-) | |
| C. | pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol•L-1 | |
| D. | 向W点所表示的1.0 L溶液中通入0.05 mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质均属于营养物质 | B. | 甲烷、乙醇、葡萄糖均属于有机物 | ||
| C. | NaOH与H2SO4均属于电解质 | D. | 纯碱、烧碱均属于碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述Ⅱ |
| A | HClO具有强氧化性 | HClO有杀菌消毒作用 |
| B | 铝比铁活泼 | 铝比铁更容易被腐蚀 |
| C | 与水反应时,钠浮在水面上 | 钠与水反应是放热反应 |
| D | 浓硝酸具有强氧化性 | 浓硝酸能和浓氨水反应产生白烟 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4g | B. | 2.8g | C. | 5.6g | D. | 11.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3的0.1mol•L-1的NaHC2O4溶液中:c(H+)=c(OH)+c(C2O42-) | |
| B. | 0.1mol•L-1的(NH4)2S溶液中:c(NH4+)=2c(S2-)+2c(HS-)+2c(H2S) | |
| C. | pH=4的CH3COOH溶液中:$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})•c(C{H}_{3}COOH)}$<1 | |
| D. | 等物质的量浓度,等体积的NaF溶液和HF溶液混合所得稀溶液中:c(H+)+c(HF)<c(F- )+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
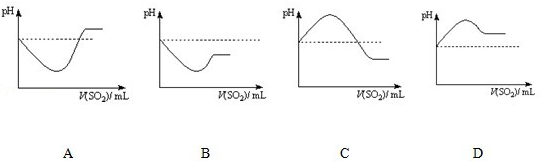
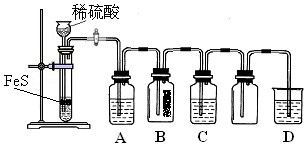 硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的很多生理过程中也起着重要作用.
硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的很多生理过程中也起着重要作用.| 资料:①H2S可溶于水(约1:2),其水溶液为二元弱酸. ②H2S可与许多金属离子反应生成沉淀. ③H2S在空气中燃烧,火焰呈淡蓝色. |
| 实验操作 | 实验现象 | |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com